2.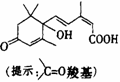 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
A.含有碳碳双键、羟基、羰基、羧基
|
C. 含有羟基、羰基、羧基、酯基
D. 含有碳碳双键、苯环、羟基、羰基
23.(9分)胃舒平主要成分是氢氧化铝,同时含有三硅镁(Mg2Si3O8`H2O)等化合物。
(1)比较铝离子和镁离子半径大小(用离子符号表示)______________________。
(2)比较铝和镁的第一电离能大小__________________(用元素符号表示)
(3)下列事实不能说明镁比铝的金属性强的是____________
A.Al(OH)3可溶于强碱溶液中,Mg(OH)2不能
B.Mg能从铝盐溶液中置换出铝
C.Mg 原子最外层只有2个电子, 而Al原子最外层有3个电子
D.Mg与盐酸反应比铝与盐酸反应更剧烈
(4)已知:电负性: Mg- 1.2 Al- 1.5 Cl-3.0 。则MgCl2晶体中存在的作用力是__________;AlBr3属于_________(填“离子”或“共价”)化合物
(5)某元素与镁元素不同周期但在相邻主族,且性质和镁元素性质十分相似,该元素符号是___________,原子核外电子排布式为_____________________。
(6) Al2O3 、MgO都有很高的熔点,都可以制耐火材料,其原因是_____________________
______________________________________________________________________________
24(12分)X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
|
Z |
Z和Y同周期,Z的电负性大于Y |
|
W |
W的一种核素的质量数为63,中子数为34 |
(1)X的最高价氧化物固态时俗称“ ”,属于 晶体。该分子的空间构型是 。
(2)Y的价层电子(外围电子)排布式为 ,Y和Z的最高价氧化物对应的水化物的酸性较强的是 (写化学式)。
(3)XY2是一种常用的溶剂,XY2的分子中存在 个σ键,属于 (填“极性”或“非极性”分子。
(4)在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(5)W的基态原子核外电子排布式是 。在W的二价硫酸盐溶液中通入过量的氨气,小心蒸发,最终得到的[W(NH3)4]SO4晶体中含有的化学键除了极性共价键外,还有 和 。
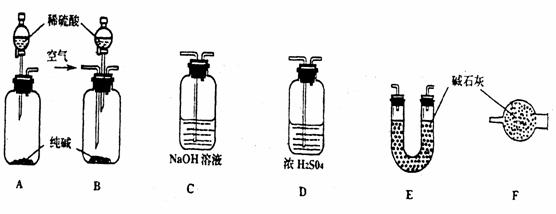
22.(9分)硅是一种重要的非金属单质,硅及其化合物的用途非常广泛。根据所学知识回答硅及其化合物的相关问题。
(1).基态硅原子的核外电子排布式为 *ks5*u 。
(2).晶体硅的微观结构与金刚石相似,晶体硅中Si-Si键之间的夹角大小约为______。
(3).下面关于SiO2晶体网状结构的叙述正确的是( )
A..最小的环上,有3个Si原子和3个O原子
B.最小的环上,有6个Si原子和6个O原子
C.存在四面体结构单元,O处于中心,Si处于4个顶角
(4)下表列有三种含硅物质(晶体)的熔点:
|
物质 |
SiO2 |
SiCl4 |
SiF4 |
|
熔点/℃ |
1610 |
-69 |
-90 |
简要解释熔点差异的原因:
①SiO2和SiCl4:__________________________________________________________;
② SiCl4和SiF4:__________________________________________________________
________________________________________________________________。
(5)“神七”字航员所穿出仓航天服是由我国自行研制的新型“连续纤维增韧”航空材料做成,其主要成分是由一种由硅及其同主族相邻短周期元素形成的化合物和碳纤维等复合而成的,它是一种新型无机非金属材料。该化合物的化学式为:________。已知该化合物的硬度仅次于金刚石,熔点比SiO2高,该化合物晶体属于________晶体[填“分子”、“原子”或“离子”。*ks5*u
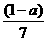 B.
B.
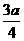 C.
C.
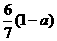 D.
D.
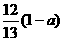
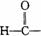

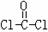 ,分子中C原子的杂化轨道方式是_____________;按原子轨道重叠方式判断COCl分子中的化学键类型为___________________。
,分子中C原子的杂化轨道方式是_____________;按原子轨道重叠方式判断COCl分子中的化学键类型为___________________。 金属铁单质的晶体在不同温度下有两种堆积方式,晶胞如图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为
。
金属铁单质的晶体在不同温度下有两种堆积方式,晶胞如图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为
。 厦门六中2010-2011学年高二(下)期中考
厦门六中2010-2011学年高二(下)期中考