22. (10分)用一种试剂鉴别MgCl2、AlCl3、FeCl2,这种试剂是 。鉴别的现象和反应的离子方程式为:
|
|
鉴别的现象 |
反应的离子方程式 |
|
MgCl2 |
|
|
|
AlCl3 |
|
|
|
FeCl2 |
|
|
19.(10分)⑴在一定条件下,下列反应达到化学平衡:
N2(g)+3H2(g)  2NH3(g);(正反应为放热反应)
2NH3(g);(正反应为放热反应)
在其它条件不变时,分别改变下列条件,对平衡的影响分别填入下表:
|
改变条件 |
对化学平衡的影响 |
|
增大压强(体积减小) |
|
|
增大N2的浓度 |
|
|
升高温度 |
|
|
使用催化剂 |
|
⑵可逆反应2 NO2 N2O4,当升高温度时,气体颜色变深,说明正反应是 热反应,当保持恒容、恒温、往密闭容器中通入稀有气体,气体的颜色
(填“变深”“变浅”或“不变”),若往此密闭容器中加水、气体的颜色
。
N2O4,当升高温度时,气体颜色变深,说明正反应是 热反应,当保持恒容、恒温、往密闭容器中通入稀有气体,气体的颜色
(填“变深”“变浅”或“不变”),若往此密闭容器中加水、气体的颜色
。
⑶已知NaClO水溶液的pH>7,说明HClO 是 酸(填“强”或“弱”),用离子方程式表示NaClO水溶液呈碱性的原因 。
|
|
Y |
Z |
|
X |
|
|
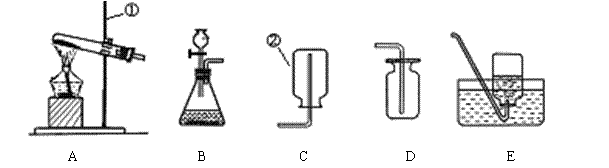 ⑴写出带标号的仪器的名称:①
;②
。
⑴写出带标号的仪器的名称:①
;②
。 ⑵实验室利用浓氨水和生石灰制取氨气应选择的装置为(填代号)
,用氯化铵与氢氧化钙制取氨气时,应选择的装置为(填代号)_______。收集氨气应装置为(填代号) 。
若要得到干燥的氨气,需用作
(填“浓硫酸”或“碱石灰”或“P2O5”)干燥剂。
⑵实验室利用浓氨水和生石灰制取氨气应选择的装置为(填代号)
,用氯化铵与氢氧化钙制取氨气时,应选择的装置为(填代号)_______。收集氨气应装置为(填代号) 。
若要得到干燥的氨气,需用作
(填“浓硫酸”或“碱石灰”或“P2O5”)干燥剂。 __________;
__________;