活动与探究:物质溶于水时温度变化。
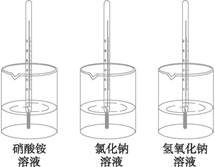
实验方案:在三只烧杯中各倒入50 mL水,用温度计测量溶解前水的温度。分别加入2药匙硝酸铵、氯化钠、氢氧化钠,搅拌,至固体全部溶解,再测量温度。(如下图)
记录:
|
|
溶解前的温度 |
溶解后的温度 |
温度的变化 |
|
水 |
25 ℃ |
25 ℃ |
无变化 |
|
溶解氯化钠 |
25 ℃ |
25 ℃ |
无变化 |
|
溶解硝酸铵 |
25 ℃ |
21 ℃ |
下降4 ℃ |
|
溶解氢氧化钠 |
25 ℃ |
36 ℃ |
上升11 ℃ |
结论:氯化钠溶于水后,溶液的温度基本不变;硝酸铵溶于水后,溶液的温度降低;氢氧化钠溶于水后,溶液的温度升高。
事实上,大多数物质溶于水后,溶液的温度基本不发生变化,如蔗糖溶液、食盐溶液。少数物质溶于水后,溶液的温度会发生变化,如大多数铵类化合物溶于水后溶液降温;氢氧化钠、浓硫酸溶于水后溶液升温。
解释:物质溶于水时,通常发生两种变化:(1)扩散过程:物质的分子或离子向水中扩散,此过程物质的分子或离子在水分子的作用下,克服分子或离子间的作用力,扩散到水中,成为自由移动的分子或离子。此过程要吸收热量。(2)水合过程:已经扩散到水中的分子或离子与水分子作用,生成水合分子或水合离子,这一过程要放出热量。
当扩散过程中吸收的热量大于水合过程中放出的热量时,溶液温度降低,如NH4NO3溶于水;当扩散过程中吸收的热量小于水合过程中放出的热量时,溶液温度升高,如NaOH、浓硫酸溶于水;当扩散过程中吸收的热量等于水合过程中放出的热量时,溶液温度不变,如NaCl溶于水。
[示例]市场上有一种俗称“摇摇冰”的罐装饮料。在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动使它们混合,罐内饮料温度就会降低。这种固体物质可能是( )
A.硝酸铵 B.烧碱 C.蔗糖 D.石灰石
解析:硝酸铵溶于水吸热,能使溶液的温度明显降低,因此,可在饮料罐的夹层中分别装入硝酸铵和水。
答案:A
 ________________+______________________
________________+______________________