19.(4分)(1)主要用到沸点、熔点。在850℃时,NaCl、KCl和Na均为熔融态,只有K为蒸气(2)利用平衡移动原理。由于钾蒸气的逸出使化学平衡向正反应方向移动,从而使反应变为现实,制得了金属钾
19.(4分)工业上生产Na、Ca、Mg等金属都用电解其熔融状态的氯化物,但制钾却不用电解熔融状态的KC1的方法制得,因为金属钾溶于熔融态的KC1中,很难得到钾。现在生产钾是用金属钠和熔化的KC1反应制取,有关数据如下:
|
|
熔点/℃ |
沸点/℃ |
密度(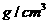 ) ) |
|
Na |
97.8 |
883 |
0.970 |
|
K |
63.7 |
774 |
0.860 |
|
NaCl |
801 |
1412 |
2.165 |
|
KCl |
770 |
1500(升华) |
1.984 |
工业生产金属钾的反应式和条件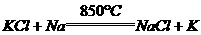 。
。
(1)工业上制金属钾主要运用上表所列的哪些物理常数?
_________________________________________________________________________。
(2)工业上制金属钾主要应用什么原理使反应变为现实?
_________________________________________________________________________。
17.(12分)下表是稀硫酸与某金属反应的实验数据:
|
实验序号 |
金属 质量/g |
金属状态 |
c(H2SO4) /mol·L-1 |
V(H2SO4) /mL |
溶液温度/℃ |
金属消失的时间/s |
|
|
反应前 |
反应后 |
||||||
|
1 |
0.10 |
丝 |
0.5 |
50 |
20 |
34 |
500 |
|
2 |
0.10 |
粉末 |
0.5 |
50 |
20 |
35 |
50 |
|
3 |
0.10 |
丝 |
0.7 |
50 |
20 |
36 |
250 |
|
4 |
0.10 |
丝 |
0.8 |
50 |
20 |
35 |
200 |
|
5 |
0.10 |
粉末 |
0.8 |
50 |
20 |
36 |
25 |
|
6 |
0.10 |
丝 |
1.0 |
50 |
20 |
35 |
125 |
|
7 |
0.10 |
丝 |
1.0 |
50 |
35 |
50 |
50 |
|
8 |
0.10 |
丝 |
1.1 |
50 |
20 |
34 |
100 |
|
9 |
0.10 |
丝 |
1.1 |
50 |
30 |
44 |
40 |
分析上述数据,回答下列问题:
(1)实验4和5表明,_________ 对反应速率有影响,_________ , 反应速率越快,能表明同一规律的实验还有_________(填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有_________(填实验序号,任填一组即可);
(3)本实验中影响反应速率的其他因素还有_________ ,其实验序号是_______(任填一组即可)。
 xC(g)达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,试回答下列有关问题:
xC(g)达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,试回答下列有关问题: B+D在四种不同条件下进行,B、D起始浓度为见反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为见反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
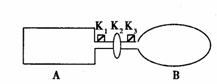 (14分)A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积相同。(已知:2NO2
(14分)A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球。关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积相同。(已知:2NO2  N2O4;△H<0)
N2O4;△H<0)