20.在10℃和4×105Pa的条件下,当反应aA(g) dD(g) + eE(g)建立平衡后,维持温度不变,逐步增大体系的压强,在不同压强下该反应建立平衡后,物质D的浓度见下表(在增大压强的过程中无其它副反应发生):
|
压强(Pa) |
4×105 |
6×105 |
1×106 |
2×106 |
|
D的浓度(mol/L) |
0.085 |
0.126 |
0.200 |
0.440 |
(1)压强从4×105 Pa增加到6×105 Pa时平衡应向 逆 反应方向移动(填“正”或 “逆”),理由是 略 。
(2)压强从1×106 Pa 增加到2×106 Pa时,平衡向 正 反应方向移动(填“正”或 “逆”).理由是 略 。
19.在100℃时,将0.1mol的四氧化二氮气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下表格:试填空:
|
时间 浓度 |
0 |
20 |
40 |
60 |
80 |
100 |
|
c(N2O4) |
0.100 |
c1 |
0.050 |
c3 |
a |
b |
|
c(NO2) |
0.000 |
0.060 |
c2 |
0.120 |
0.120 |
0.120 |
(1)该反应的化学方程式__ N2O4
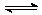 _2NO2_____________;达到平衡时四氧化二氮的转化率为____60%______。表中c2__>___c3__=___a__=____b(选填“>”、“<”、“=”)。
_2NO2_____________;达到平衡时四氧化二氮的转化率为____60%______。表中c2__>___c3__=___a__=____b(选填“>”、“<”、“=”)。
(2)20s时四氧化二氮的浓度c1=__0.07_mol·L-1 ,在0s~20s内四氧化二氮的平均反应速率为__0.0015____mol·(L·s)-1。
 (3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是_____0.2____ mol·L-1。
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是_____0.2____ mol·L-1。
 cC(固)+dD当反应进行一定时间后,测得A减少了n摩,B减少了
cC(固)+dD当反应进行一定时间后,测得A减少了n摩,B减少了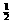 n摩,C增加了
n摩,C增加了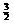 n 摩,D增加了n摩,此时达到化学平衡:
n 摩,D增加了n摩,此时达到化学平衡: 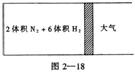 在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生以下反应: N2+3H2
在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通容器中发生以下反应: N2+3H2  2NH3+Q若反应达到平衡后,测得混合气体为7体积。据此回答下列问题:
2NH3+Q若反应达到平衡后,测得混合气体为7体积。据此回答下列问题: pC达到平衡,若:
pC达到平衡,若: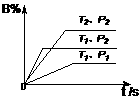 反应 X(气)+ Y(气)
反应 X(气)+ Y(气)  (CH3COOH)2(气)+热。现欲测定乙酸的分子量,应采用的反应条件是:
(CH3COOH)2(气)+热。现欲测定乙酸的分子量,应采用的反应条件是: 某固定体积的密闭容器中存在化学平衡:a A(气)
某固定体积的密闭容器中存在化学平衡:a A(气)