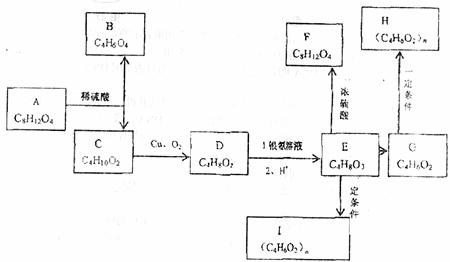
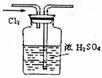
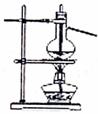
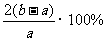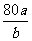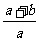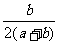28.(18分)I、目前,我国采用“接触法”制硫酸,生产设备如图所示:
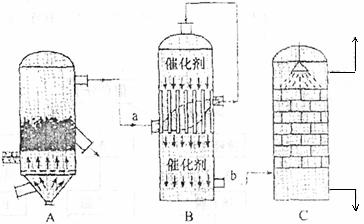
(1)图中设备A的名称是 ,a、b两处所含气体的化学式分别为 、 。
(2)有关接触法制硫酸的下列说法中,不正确的是 。
A.二氧化硫的接触氧化在合成塔中发生
B.吸收塔得到的硫酸浓度为98%
C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失4%
D.B装置中反应的条件之一为较高温度是为了提高SO2的转化率
|
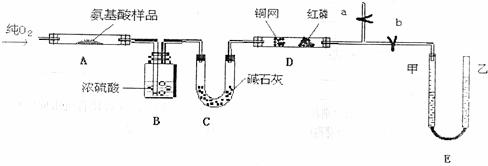
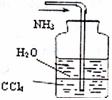
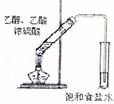
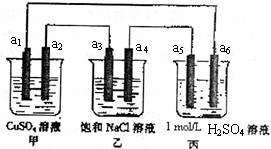
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通入一段时间的氧气,这样做的目的是 ,之后关闭止水夹a。
(2)E装置的作用是测量 的体积,在读反应前后甲管中液面的读数求其差值的过程中,应注意 (填代号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(3)严格地说,按上述方案只能确定氨基酸的 。
若要确定此氨基酸的分子式,来要测定该氨基酸的 。
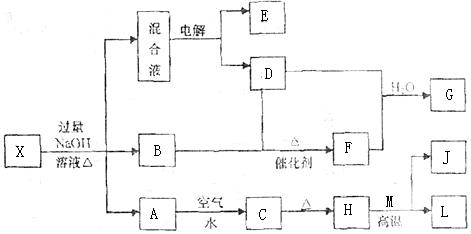
26.(13分)有原子序数依次增大的六种短周期主族元素A、B、C、D、E、F。其中A与D、B与E分别同主族,B原子最外层电子数为内层电子数的2倍;F元素的原子半径在所在周期的主族元素中最小;C与A、D都可形成两种化合物,且所形成的化合物中各有一种具有漂白性。B、E分别与C形成的化合物晶体类型不同。试回答下列问题:
(1)C、D以原子个数比为1:1形成的化合物的电子式为
(2)E单质的晶体类型是 。
(3)试写出工业用电解溶液法得到单质F的离子方程式:
(4)写出以上六种元素形成的含18个电子的分子式 (任写三种)。
(5)已知几种元素之间形成的化学键的键能如下:
|
化学键 |
A-A |
A-F |
B-E |
C-E |
E-E |
E-F |
|
键能(kJ/mol) |
436 |
431 |
347 |
460 |
176 |
360 |
工业上用含有E、F两种元素(原子个数比为1:4)的化合物在高温下与A单质反应来得到高纯度的单质E。则该反应的热化学方程式为 。
9.下表中的实验,“操作和现象”与“结论”对应关系正确的是 ( )
|
|
操作和现象 |
结论 |
|
A |
向纯碱中滴加足量浓盐酸,将所得气体通入苯酚溶液中,溶液变浑浊 |
酸性:盐酸>碳酸>苯酚 |
|
B |
取某溶液少量,加入盐酸酸化的BaCl2溶液,出现白色沉淀 |
该溶液中一定含有大量的SO42- |
|
C |
取少量Fe(NO3)2试样加水溶液后加稀H2SO4酸化,滴加KSCN溶液,溶液变为红色 |
该Fe(NO3)2试样已经变质 |
|
D |
取皂化反应后的混合液滴入盛水的烧杯中,在液体表面出现油滴 |
皂化反应不完全 |