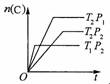
16.有关X、Y、Z、W四种金属进行如下实验:
|
1 |
将X和Y用导线连接,浸入电解质溶液中,Y不易腐蚀 |
|
2 |
将片状的X、W分别投入等浓度盐酸中都有气体产生,W比X反应剧烈 |
|
3 |
用惰性电极电解等物质的量浓度的Y和Z的硝酸盐混合溶液,在阴极上首先析出单质Z |
根据以下事实,下列判断或推测错误的是
A.Z的阳离子氧化性最强
B.W的还原性强于Y的还原性
C.Z放入CuSO4溶液中一定有Cu析出
D.用X、Z和稀硫酸可构成原电池,且X做负极
第Ⅱ卷(非选择题 共60分)
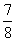 ,则C的转化率为
。
,则C的转化率为
。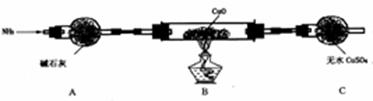
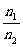 的值是
的值是 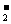 +H2↑
+H2↑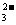 +2HClO
+2HClO Fe(OH)3+3H+
Fe(OH)3+3H+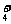 、Na+、Cl-、SCN-
、Na+、Cl-、SCN-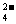 、NO
、NO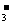
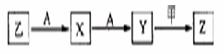
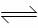 zC(g);△H=a。将xmolA和ymolB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)与反应时间(t)的关系如图所示。下列判断正确的是
zC(g);△H=a。将xmolA和ymolB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)与反应时间(t)的关系如图所示。下列判断正确的是