网址:http://m.1010jiajiao.com/timu_id_1740440[举报]
(10分)A、B、C、D四种元素的原子序数均小于18,其最高正价数依次为1,4,5,7,已知B的原子核外次外层电子数为2。A、C原子的核外次外层电子数为8。D元素的最高价氧化物对应的水化物是已知含氧酸中最强酸,则:
(1)A的离子结构示意图是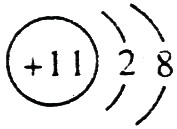 ,C的原子结构示意图是
,C的原子结构示意图是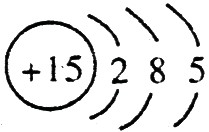 。
。
(2)C的最高价氧化物对应的水化物与A的氢氧化物生成三种盐,化学式分别为Na3PO4、Na2HPO4、NaH2PO4。
(3)C、D的气态氢化物稳定性由强到弱的顺序是 HCl>PH3。
【解析】 最高正价=原子最外层电子数,B元素的原子最外层电子数应为4,B元素原子的次外层电子数为2,为K层,B元素原子核外共有2+4=6个电子,B是6号元素碳;A、C原子次外层电子数为8,则A、C原子核外电子数分别是:2+8+1=11和2+8+5=15,所以A为11号元素钠,C为15号元素磷;在1~18号元素中,最高价为+7的只有氯元素(F无正价),而HClO4是已知含氧酸中最强的酸,故D为氯。
(1)钠总是+1价,其离子结构示意图为: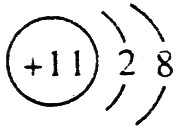 ;磷的原子序数是15,其原子结构示意图是:
;磷的原子序数是15,其原子结构示意图是: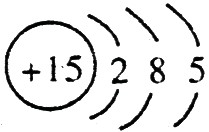 。
。
(2)磷的最高价(+5)氧化物对应的水化物是H3PO4,与NaOH反应生成:Na3PO4、NaH2PO4三种盐。
(3)P、Cl原子都具有3个电子层,核电荷数P(15)小于Cl(17),原子半径r(P)>r(Cl),所以非金属Cl>P,气态氢化物稳定性HCl>PH3。
查看习题详情和答案>>图表法、图象法是常用的科学研究方法.下表列出前20号元素中的某些元素性质的一些数据:
| 元素 性质 |
A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中第一电离能最小的是:
(2)由上述C、E、G三种元素中的某两种元素形成的化合物中,每个原子的最外层都满足8电子稳定结构的可能是
(3)元素E与C及氢元素可形成一种相对分子质量为60的一元羧酸分子.其分子中共形成
(4)短周期某主族元素K的电离能情况如图(A)所示.则K元素位于周期表的第

图B是研究部分元素的氢化物的沸点变化规律的图象,折线c可以表达出第
(17分)
优良的有机溶剂对孟烷、耐热型特种高分子功能材料PMnMA的合成路线如下:
己知芳香化合物苯环上的氢原子可被卤代烷中的烷基取代。如:
(1)B为芳香烃。
①由B生成对孟烷的反应类型是
②(CH3 )2CHCl与A生成B的化学方程武是
③A的同系物中相对分子质量最小的物质是
(2) 1.08g的C与饱和溴水完全反应生成3.45 g白色沉淀。E不能使Br2的CC14溶液褪色.
①F的官能团是
②C的结构简式是
③反应I的化学方程式是
(3)下列说法正确的是(选填字母)
a. B可使酸性高锰放钾溶液褪色 b. C不存在醛类同分异构体
c. D的酸性比E弱 d. E的沸点高于对孟烷
(4) G的核磁共振氢谱有3种峰,其峰面积之比为3:2:1。G与NaHCO3反应放出CO2。反应II的化学方程式是
查看习题详情和答案>>
(17分)
优良的有机溶剂对孟烷、耐热型特种高分子功能材料PMnMA的合成路线如下:
己知芳香化合物苯环上的氢原子可被卤代烷中的烷基取代。如:
(1)B为芳香烃。
①由B生成对孟烷的反应类型是
②(CH3 )2 CHCl与A生成B的化学方程武是
③A的同系物中相对分子质量最小的物质是
(2) 1.08g的C与饱和溴水完全反应生成3.45 g白色沉淀。E不能使Br2的CC14溶液褪色.
①F的官能团是
②C的结构简式是
③反应I的化学方程式是
(3)下列说法正确的是(选填字母)
a. B可使酸性高锰放钾溶液褪色 b. C不存在醛类同分异构体
c. D的酸性比E弱 d. E的沸点高于对孟烷
(4) G的核磁共振氢谱有3种峰,其峰面积之比为3:2:1。G与NaHCO3反应放出CO2。反应II的化学方程式是
(17分)
优良的有机溶剂对孟烷、耐热型特种高分子功能材料PMnMA的合成路线如下:

己知芳香化合物苯环上的氢原子可被卤代烷中的烷基取代。如:

(1)B为芳香烃。
①由B生成对孟烷的反应类型是
②(CH3 )2 CHCl与A生成B的化学方程武是
③A的同系物中相对分子质量最小的物质是
(2) 1.08g的C与饱和溴水完全反应生成3.45 g白色沉淀。E不能使Br2的CC14溶液褪色.
①F的官能团是
②C的结构简式是
③反应I的化学方程式是
(3)下列说法正确的是(选填字母)
a. B可使酸性高锰放钾溶液褪色 b. C不存在醛类同分异构体
c. D的酸性比E弱 d. E的沸点高于对孟烷
(4) G的核磁共振氢谱有3种峰,其峰面积之比为3:2:1。G与NaHCO3反应放出CO2。反应II的化学方程式是
查看习题详情和答案>>