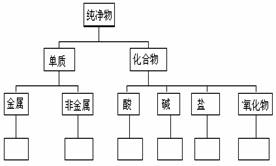
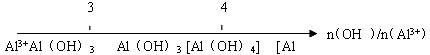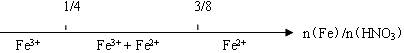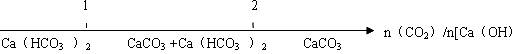15.LiAlH4(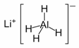 )、LiH是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是 ( )
)、LiH是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是 ( )
A.LiH与D2O反应,所得氢气的摩尔质量为4g/mol
B.1molLiAlH4在125℃完全分解,转移3mol电子
C.LiAlH4溶于适量水得到无色溶液,则化学方程式可表示为:LiAlH4+2H2O=LiAlO2+4H2↑
D.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
第Ⅱ卷(非选择题 共55分)
|
 12Na2CrO4 + 3Fe2O3
+7KCl + 12H2O,
12Na2CrO4 + 3Fe2O3
+7KCl + 12H2O,
试回答下列问题
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
。
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式: 。
(3)操作③的目的是什么,用简要的文字说明: 。
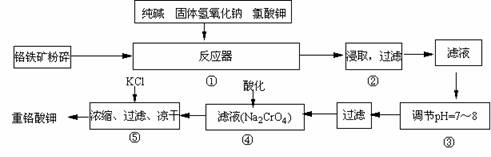
(4)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
。
(5)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
判断达到滴定终点的依据是: 。
10.氮化铝(AlN)广泛用于电子工业、陶瓷工业等领域。可通过如下反应制取:
Al2O3+N2+3C 2AlN+3CO
2AlN+3CO
|
A.该反应中,Al2O3是氧化剂 B.该反应中,N2是还原剂
C.该反应中,C是还原剂 D.该反应中每生成2mol AlN,N2得到3mol e-
8.离子检验的常用方法有三种:
|
检验方法 |
沉淀法 |
显色法 |
气体法 |
|
含义 |
反应中有沉淀产生或溶解 |
反应中有颜色变化 |
反应中有气体产生 |
下列离子检验的方法不合理的是 ( )
A.NH4+-气体法 B.I--沉淀法 C.Fe3+-显色法 D.Ca2+-气体法