14.设NA为阿伏加德罗常数的值.下列有关说法正确的是( )
| A. | 32gCu在足量O2或硫蒸气中完全燃烧失去的电子数均为NA | |
| B. | 4g甲烷和8g甲醇含有的氢原子数均为NA | |
| C. | 标准状况下,5.6L乙烷中含有的共价键数目为1.5NA | |
| D. | 一定条件下,32gSO2与足量O2反应,转移电子数为NA |
13.化学在生产、生活中有着广泛的应用,下列物质的化学性质与应用的对应关系正确的是( )
| 化学性质 | 应用 | |
| A | O价铁具有还原性 | 铁粉可用于食品中的脱氧剂 |
| B | 明矾与NaOH生成Al(OH)3 | 明矾可作净水剂 |
| C | Fe的金属性比Cu活泼 | FeCl3浓溶液腐蚀Cu刻制印刷电路板 |
| D | NaHCO3水解显碱性 | 发酵粉中含有NaHCO3 |
| A. | A | B. | B | C. | C | D. | D |
12.下列实验现象正确且实验操作能达到实验目的是( )
| 实验操作 | 实验现象 | 实验目的 | |
| A | 向待测液中滴加盐酸和稀硝酸 | 产生白色沉淀 | 检验待测液中是否含有Ag+ |
| B | 将含有少量CO2的CO气体緩缓通过足量的 过氧化钠粉末 | 淡黄色粉末变白 | 除去CO2,提纯CO |
| C | 在Na2S溶液中滴加新制氯水 | 产生浅黄色沉淀 | 证明氯的非金属性比硫的强 |
| D | 在Ag2S浊液中滴加NaCl溶液 | 产生白色沉淀 | 比较Ag2S和AgCl的溶解度大小 |
| A. | A | B. | B | C. | C | D. | D |
11.设NA为阿伏伽德罗常数的值.下列有关叙述正确的是( )
| A. | 28 g乙烯和甲烷混合气体中的氢原子数为4NA | |
| B. | 标准状况下,11.2 LCH2Cl2含有的共价键数为2NA | |
| C. | 1mol SO2与 l mol O2反应生成的SO3分子数为NA | |
| D. | 过量铜与含0.4 molHNO3的浓硝酸反应,电子转移数大于0.2NA |
10.化学与生活、生产密切相关,下列有关说法错误的是( )
| A. | 碘酒能使蛋白质变性,涂在人体皮肤上可杀菌消毒 | |
| B. | 大米、小米、马铃薯中均含有淀粉,可为人体活动提供能量 | |
| C. | 食盐、糖、醋可作调味剂,不可用作食品防腐剂 | |
| D. | 船帕外壳装上锌块防腐,采用的是牺牲阳极的阴极保护法 |
7.实验室以蛇纹石酸浸出液(主要含Fe3+,还有一定量的Al3+、Mn2+、Ca2+、Mg2+等)为原料制备高纯氧化铁,流程如图1:
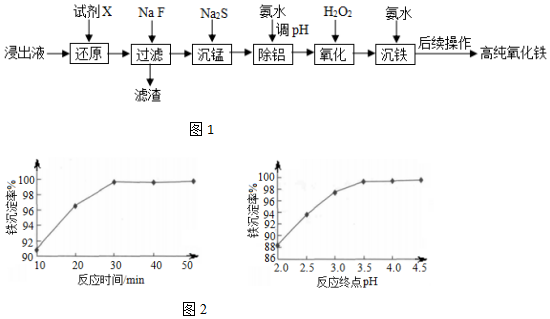
已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
(1)“还原”时,应选择C(填字母).
A.Zn粉 B.NaClO溶液 C.Fe粉
(2)“滤渣”的主要成分除含有少量MnF2外,还含有CaF2、MgF2(填化学式).
(3)“沉锰”时,已知:Ksp(MnS)=4.65×10-14.为确保沉锰完全[即溶液中c(Mn2+)<1.0×10-6 mol•L-1],应保持溶液中c(S2-)>4.65×10-8mol•L-1mol•L-1.
(4)“除铝”时,控制溶液pH的范围为5.0~5.8.
(5)“氧化”时,常用酸性K2Cr2O7溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为Cr2O72-+14H++6Fe2+═2Cr3++6Fe3++7H2O.
(6)“沉铁”时,反应温度为85℃条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是反应时间30min、终点pH=3.5.

已知流程中相关金属离子生成氢氧化物沉淀的pH如表:
| 氢氧化物 | Fe3+ | Fe2+ | Al3+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 |
| 沉淀完全的pH | 3.2 | 8.8 | 5.0 |
A.Zn粉 B.NaClO溶液 C.Fe粉
(2)“滤渣”的主要成分除含有少量MnF2外,还含有CaF2、MgF2(填化学式).
(3)“沉锰”时,已知:Ksp(MnS)=4.65×10-14.为确保沉锰完全[即溶液中c(Mn2+)<1.0×10-6 mol•L-1],应保持溶液中c(S2-)>4.65×10-8mol•L-1mol•L-1.
(4)“除铝”时,控制溶液pH的范围为5.0~5.8.
(5)“氧化”时,常用酸性K2Cr2O7溶液检测是否残留未被氧化的金属离子,该反应的离子方程式为Cr2O72-+14H++6Fe2+═2Cr3++6Fe3++7H2O.
(6)“沉铁”时,反应温度为85℃条件下,反应时间和反应终点pH对铁的沉淀率的影响分别如图2所示,则最佳的工艺条件是反应时间30min、终点pH=3.5.
6.下列图示与对应的叙述相符合的是( )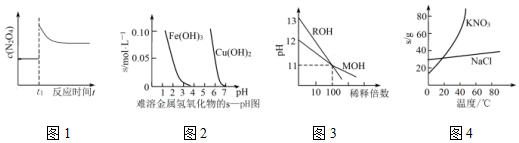

| A. | 图1表示平衡2NO2(g)?N2O4(g)在t1时迅速将体积缩小后c(N2O4)的变化 | |
| B. | 图2表示除去CuSO4溶液中的Fe3+可采用加入CuO调节溶液pH到4~5 | |
| C. | 图3表示MOH和ROH两种一元碱的溶液分别加水稀释时的pH变化,则碱性:MOH>ROH | |
| D. | 图4为KNO3和NaCl溶解度曲线,若除去NaCl中少量的KNO3,可在较高温度下制得浓溶液后,再冷却结晶、过滤、洗涤、干燥得纯净NaCl |
5. 化学上常用AG表示溶液中的lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.25℃时,用0.100mol•L-1的NaOH溶液滴定20.00mL 0.100mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
化学上常用AG表示溶液中的lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.25℃时,用0.100mol•L-1的NaOH溶液滴定20.00mL 0.100mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
0 163013 163021 163027 163031 163037 163039 163043 163049 163051 163057 163063 163067 163069 163073 163079 163081 163087 163091 163093 163097 163099 163103 163105 163107 163108 163109 163111 163112 163113 163115 163117 163121 163123 163127 163129 163133 163139 163141 163147 163151 163153 163157 163163 163169 163171 163177 163181 163183 163189 163193 163199 163207 203614
 化学上常用AG表示溶液中的lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.25℃时,用0.100mol•L-1的NaOH溶液滴定20.00mL 0.100mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )
化学上常用AG表示溶液中的lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.25℃时,用0.100mol•L-1的NaOH溶液滴定20.00mL 0.100mol•L-1的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法正确的是( )| A. | D点溶液的pH=11.25 | |
| B. | B点溶液中存在 c(H+ )-c(OH- )=c(NO2- )-c(HNO2) | |
| C. | C点时,加入NaOH溶液的体积为20 mL | |
| D. | 25℃时,HNO2的电离常数Ka=1.0×10-55 |
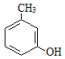 +CH3COCH2COOC2H5$→_{10℃搅拌12h}^{浓硫酸}$
+CH3COCH2COOC2H5$→_{10℃搅拌12h}^{浓硫酸}$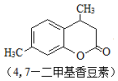 +C2H5OH+H2O
+C2H5OH+H2O