题目内容
13.化学在生产、生活中有着广泛的应用,下列物质的化学性质与应用的对应关系正确的是( )| 化学性质 | 应用 | |
| A | O价铁具有还原性 | 铁粉可用于食品中的脱氧剂 |
| B | 明矾与NaOH生成Al(OH)3 | 明矾可作净水剂 |
| C | Fe的金属性比Cu活泼 | FeCl3浓溶液腐蚀Cu刻制印刷电路板 |
| D | NaHCO3水解显碱性 | 发酵粉中含有NaHCO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.铁粉具有还原性,能够与氧气反应;
B.明矾与氢氧化钠反应不能产生氢氧化铝胶体;
C.Cu与氯化铁反应反应生成氯化铜、氯化亚铁,Cu失去电子;
D.发酵粉中含有碳酸氢钠,是利用其不稳定性.
解答 解:A.铁粉具有还原性,能够与氧气反应,放入食品袋中可以防止食品氧化变质,故A正确;
B.明矾与少量氢氧化钠反应生成氢氧化铝沉淀,与过量氢氧化钠反应生成偏铝酸钠,而明矾净水是铝离子水解生成的氢氧化铝胶体有吸附悬浮杂质的作用,故B错误;
C.Cu与氯化铁反应反应生成氯化铜、氯化亚铁,Cu失去电子,与Fe、Cu活泼性无关,故C错误;
D.碳酸氢钠水解呈碱性,但发酵粉中使用碳酸氢钠是因为碳酸氢钠受热时不稳定的性质,故D错误;
故选A.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
3.联苯(结构如图所示 ),碳碳单键可以旋转)的二氯代物有( )
),碳碳单键可以旋转)的二氯代物有( )
 ),碳碳单键可以旋转)的二氯代物有( )
),碳碳单键可以旋转)的二氯代物有( )| A. | 9种 | B. | 12种 | C. | 20种 | D. | 24种 |
4.在光照条件下,将等物质的量的甲烷和氯气混合,充分反应后,得到产物的物质的量最多的是( )
| A. | CH3Cl | B. | CHCl3 | C. | CCl4 | D. | HCl |
1.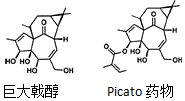 2016 年化学领域重要成果之一是丹麦制药公司LEO Pharma与美国斯克里普斯研究所(The Scripps Research Institute)的Phil S.Baran课题组合作,成功地将合成巨大戟醇(一个分子中含有20个碳原子)的步骤由37步缩短至14步.巨大戟醇是合成治疗日光性角化病药物(Picato)的原料.下列说法错误的是( )
2016 年化学领域重要成果之一是丹麦制药公司LEO Pharma与美国斯克里普斯研究所(The Scripps Research Institute)的Phil S.Baran课题组合作,成功地将合成巨大戟醇(一个分子中含有20个碳原子)的步骤由37步缩短至14步.巨大戟醇是合成治疗日光性角化病药物(Picato)的原料.下列说法错误的是( )
 2016 年化学领域重要成果之一是丹麦制药公司LEO Pharma与美国斯克里普斯研究所(The Scripps Research Institute)的Phil S.Baran课题组合作,成功地将合成巨大戟醇(一个分子中含有20个碳原子)的步骤由37步缩短至14步.巨大戟醇是合成治疗日光性角化病药物(Picato)的原料.下列说法错误的是( )
2016 年化学领域重要成果之一是丹麦制药公司LEO Pharma与美国斯克里普斯研究所(The Scripps Research Institute)的Phil S.Baran课题组合作,成功地将合成巨大戟醇(一个分子中含有20个碳原子)的步骤由37步缩短至14步.巨大戟醇是合成治疗日光性角化病药物(Picato)的原料.下列说法错误的是( )| A. | 由巨大戟醇制备Picato药物的另一种反应物是(CH3)2C=CHCOOH | |
| B. | 巨大戟醇能发生取代反应、氧化反应、加成反应 | |
| C. | 巨大戟醇和Picato药物都不属于芳香族化合物 | |
| D. | 0.1mol巨大戟醇完全燃烧消耗2.45molO2 |
18.下列实验操作能得出相应结论的是( )
| 选项 | 操作或现象 | 结论 |
| A | 向含有NaOH的Mg(OH)2悬浊液中滴加CoCl2溶液,产生粉色沉淀 | KSP[Co(OH)2]<KSP[Mg(OH)2] |
| B | 将铁粉和铜粉分别和硫粉混合加热,分别生成FeS、Cu2S | 还原性:Fe>Cu |
| C | 在透明溶液中通入CO2,产生白色胶状物质 | 原溶液含有SiO32- |
| D | 控制其它条件相同,在过氧化氢中分别加入等量的氯化铁和氯化铜做催化剂,加入氯化铁的产生气泡速率更快 | 其它条件相同时,Fe3+对过氧化氢分解的催化作用强于Cu2+ |
| A. | A | B. | B | C. | C | D. | D |
5.苹果酸的结构简式为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 1mol苹果酸与足量金属Na反应生成生成lmolH2 | |
| B. | 1mol苹果酸可与3molNaOH发生中和反应 | |
| C. | 苹果酸中能发生酯化反应的官能团有2种 | |
| D. |  与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
2.化学来源于生活,又服务于生活.下列说法正确的是( )
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 聚氯乙烯塑料广泛应用于塑料薄膜、食品包装袋等 | |
| C. | 高铁车厢材料大部分采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强 | |
| D. | 氢氧燃料电池、硅太阳能电池都利用了原电池原理 |
16.下列实验操作和现象对应的结论错误的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向溶液X中滴加BaCl2溶液,有白色沉淀生成 | 溶液X中可能含有SO42- |
| B |  | 反应结束后,锥形瓶中溶液的溶质是Cu(NO3)2、CuSO4,集气瓶中收集到的气体是NO |
| C | 向1mL浓度均为0.05mol•L-l NaCl、NaI的混合溶液中滴加2滴0.01mol•L-lAgNO3溶液,振荡,沉淀呈黄色 | Ksp (AgCl)>Ksp(AgI) |
| D | 室温下,用pH试纸测得0.1mol•L-1 NaHSO3溶液的pH约为5 | HSO3-的电离程度大于其水解程度 |
| A. | A | B. | B | C. | C | D. | D |