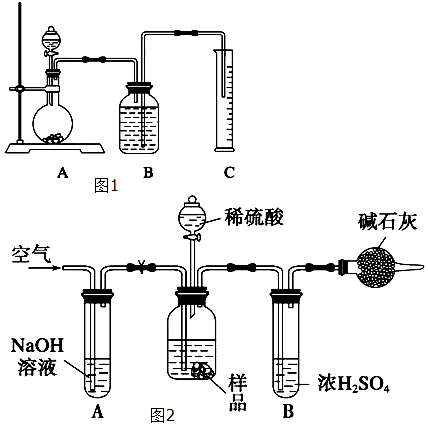
17.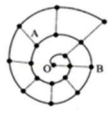 某同学在研究前 18 号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧 线上的“.”代表一种元素,其中 O 点代表氢元素.下列说法中错误的是( )
某同学在研究前 18 号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧 线上的“.”代表一种元素,其中 O 点代表氢元素.下列说法中错误的是( )
 某同学在研究前 18 号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧 线上的“.”代表一种元素,其中 O 点代表氢元素.下列说法中错误的是( )
某同学在研究前 18 号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧 线上的“.”代表一种元素,其中 O 点代表氢元素.下列说法中错误的是( )| A. | B 元素是图中金属性最强的元素 | |
| B. | 虚线相连的元素处于同一族 | |
| C. | 离 O 点越远的元素原子半径越大 | |
| D. | A、B 两种元素组成的化合物中可能含有共价键 |
16.已知短周期元素的离子aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子半径 A>B>D>C | B. | 原子序数 D>C>B>A | ||
| C. | 离子半径 C>D>B>A | D. | 单质的还原性 A>B>D>C |
14.如图所示,△H1=-393.5kJ•mol-1,△H2=-395.4kJ•mol-1,下列说法或表示式正确的是( )


| A. | 石墨和金刚石互为同位素 | |
| B. | 金刚石的总能量比石墨的总能量高1.9 kJ | |
| C. | C(石墨)═C(金刚石)△H=+1.9 kJ•mol-1 | |
| D. | C(s,石墨)═C(s,金刚石)△H=+1.9 kJ•mol-1 |
13.下列与化学实验有关的说法中,正确的是( )
| A. | 酸式滴定管可以用来装所有的酸或酸性溶液 | |
| B. | 灼烧Na2CO3•10H2O 晶体时应选用耐高温的石英坩埚 | |
| C. | 实验室制取乙酸乙酯时用饱和NaHCO3溶液收集产物 | |
| D. | 测定溶液的pH时,在玻璃板上放一片干燥的pH试纸,用玻璃棒蘸取取待试液滴到pH试纸上,把试纸与标准比色卡比较,读出溶液的pH |
12.利用如图装置进行实验,下列有关实验操作和现象正确的是( )
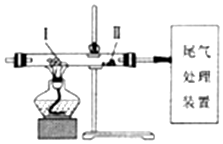

| A. | 缓慢通入N2,再加热Ⅰ处的碳酸氢钠,可观察到Ⅱ处过氧化钠粉末由浅黄色变成白色 | |
| B. | 缓慢通入N2,加热Ⅰ处KClO3和MnO2的混合物,可观察到Ⅱ处干燥KI淀粉试纸变成蓝色 | |
| C. | 先对Ⅰ处的氯化铵加热,再缓慢通入N2,可看到Ⅰ处固体减少,Ⅱ处无固体沉积 | |
| D. | 先缓慢通入CO2,再加热Ⅰ处炭粉,可观察到Ⅱ处氧化铁粉末由红色变成黑色 |
9.甲、乙、丙三瓶等体积的新制氯水,浓度均为0.1mol•L-1.如果在甲瓶中加入少量的CaCO3晶体(m mol),在乙瓶中加入少量CaSO3晶体(m mol),丙瓶不变,片刻后,甲、乙、丙三瓶溶液中HClO的物质的量的浓度大小关系是(溶液体积变化忽略不计)( )
0 162624 162632 162638 162642 162648 162650 162654 162660 162662 162668 162674 162678 162680 162684 162690 162692 162698 162702 162704 162708 162710 162714 162716 162718 162719 162720 162722 162723 162724 162726 162728 162732 162734 162738 162740 162744 162750 162752 162758 162762 162764 162768 162774 162780 162782 162788 162792 162794 162800 162804 162810 162818 203614
| A. | 甲=乙>丙 | B. | 丙>甲=乙 | C. | 甲>乙>丙 | D. | 甲>丙>乙 |
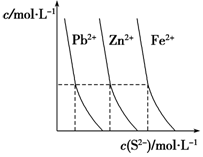 高中化学涉及的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡等,它们在工农业生产中都有广泛的应用.请回答下列问题:
高中化学涉及的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡等,它们在工农业生产中都有广泛的应用.请回答下列问题: