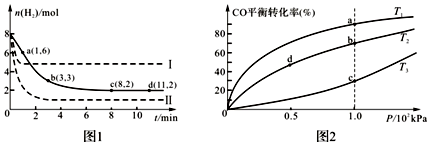
11.某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气.为了验证哪位同学的判断正确,丙同学设计了如图1所示实验装置(锌与浓硫酸共热时产生的气体为X,气体发生装置略去).试回答:
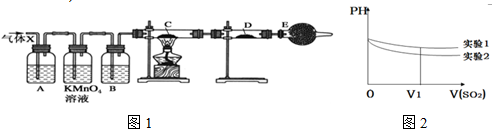
(1)上述反应中生成二氧化硫的化学方程式为Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O.
(2)乙同学认为还可能产生氢气的理由是在Zn与浓H2SO4反应过程中,H2SO4被消耗且有水生成,H2SO4浓度逐渐减小,变成稀硫酸,Zn与稀H2SO4反应生成H2.
(3)A中加入的试剂可能是品红溶液,作用是检验SO2;B中加入的试剂可能是浓H2SO4,作用是吸收水蒸气;
(4)可以证明气体X中含有氢气的实验现象是:C中:黑色(CuO)粉末变成红色(Cu),D中:白色粉末变成蓝色.
(5)II.该小组同学将收集的SO2气体通入0.1mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
该小组设计实验验证了假设一,
(5)请在下表空白处填写相关实验现象
(6)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图2,实验1中溶液pH变小的原因是SO2溶于水后生成H2SO3,亚硫酸显酸性,故pH值减小V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)3SO2+2H2O+2NO3- 2NO+4H++3SO42-;.
2NO+4H++3SO42-;.

(1)上述反应中生成二氧化硫的化学方程式为Zn+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ZnSO4+SO2↑+2H2O.
(2)乙同学认为还可能产生氢气的理由是在Zn与浓H2SO4反应过程中,H2SO4被消耗且有水生成,H2SO4浓度逐渐减小,变成稀硫酸,Zn与稀H2SO4反应生成H2.
(3)A中加入的试剂可能是品红溶液,作用是检验SO2;B中加入的试剂可能是浓H2SO4,作用是吸收水蒸气;
(4)可以证明气体X中含有氢气的实验现象是:C中:黑色(CuO)粉末变成红色(Cu),D中:白色粉末变成蓝色.
(5)II.该小组同学将收集的SO2气体通入0.1mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
该小组设计实验验证了假设一,
(5)请在下表空白处填写相关实验现象
| 实验步骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的25ml0.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | 假设一成立 | |
| 实验2:在盛有不含O2的25ml0.1mol/LBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 |
 2NO+4H++3SO42-;.
2NO+4H++3SO42-;.
10.下列过程中,最终的白色沉淀不一定是BaSO4的是( )
| A. | Ba(NO3)2溶液$\stackrel{通入SO_{2}}{→}$白色沉淀 | |
| B. | 无色溶液$\stackrel{稀HNO_{3}}{→}$ $\stackrel{BaCl_{2}溶液}{→}$白色沉淀 | |
| C. | Ba(NO3)2溶液$\stackrel{加过量HCl}{→}$无现象 $\stackrel{Na_{2}SO_{4}}{→}$白色沉淀 | |
| D. | Fe(NO3)2溶液$\stackrel{加过量HCl}{→}$ $\stackrel{通入SO_{2}}{→}$ $\stackrel{BaCl_{2}}{→}$白色沉淀 |
9.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 将1molCl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA | |
| B. | 12gNaHSO4固体中含阳离子数为0.1NA | |
| C. | 标准状况下,22.4LBr2中所含分子数为NA | |
| D. | 7.8gNa2O2与足量的水反应转移电子数为0.2NA |
8.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 常温下将Cu放入浓H2SO4中 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | 向某溶液中加入CCl4,振荡后静置 | 液体分层,下层呈紫红色 | 该溶液中存在I- |
| C | 向1.0mol•L-1的NaHCO3溶液中滴加2滴甲基橙 | 溶液呈黄色 | NaHCO3溶液呈碱性 |
| D | 向浓度均为0.1mol•L-1的Al2(SO4)3、Fe2(SO4)3的溶液中逐滴加入氨水 | 先有红褐色沉淀生成,后有白色沉淀生成 | Al(OH)3 的溶度积比Fe(OH)3的大 |
| A. | A | B. | B | C. | C | D. | D |
6.Mg-AgCl 电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+Mg═Mg2++2Ag+2Cl-.有关该电池的说法正确的是( )
| A. | Mg 为电池的正极 | |
| B. | 负极反应为 AgCl+e-=Ag+Cl- | |
| C. | 可用于海上应急照明供电 | |
| D. | 电池工作时,电解质溶液质量不断减轻 |
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 无色中性溶液中:Na+、K+、CO32-、SO42- | |
| B. | 含有大量Fe3+的溶液中:Na+、Mg2+、NO3-、I- | |
| C. | 加入铝粉后有气体放出的溶液:Fe2+、K+、NO3-、Cl- | |
| D. | 能使酚酞变红色的溶液:CO32-、Cl-、F-、K+ |
4.化学与生活、社会发展息息相关,下列说法正确的是( )
| A. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| B. | 用乙醚从黄花蒿中提取青蒿素是利用了氧化还原反应原理 | |
| C. | “丹砂(HgS)烧之成水银,积变又成丹砂.”这个过程是可逆反应 | |
| D. | 丁达尔效应可用于区别溶液与胶体,云、雾、稀硫酸均能产生丁达尔效应 |
3.草酸钴可用于指示剂和催化剂的制备.用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取CoC2O4•2H2O工艺流程如图:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3的主要目的是将Co3+、Fe3+还原为Co2+、Fe2+.
(2)向浸出液中加入NaClO3的离子反应方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)已知:常温下
NH3•H2O?NH4++OH- Kb=1.8×10-5
H2C2O4?H++HC2O4- Ka1=5.4×10-2
HC2O4-?H+C2O42- Ka2=5.4×10-5
则该流程中所用(NH4)2C2O4溶液的pH<7(填“>”或“<”或“=”).
(4)加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时可选用的试剂有:A.
A.蒸馏水B.自来水C.饱和的(NH4)2C2O4溶液D.稀盐酸
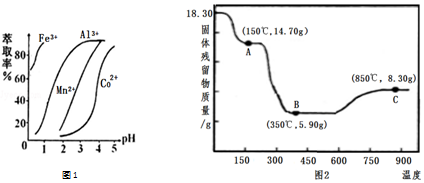
(5)萃取剂对金属离子的萃取率与pH的关系如右图1,萃取剂的作用是除去溶液中的Mn2+;其使用的适宜pH范围是B.
A.2.0~2.5B.3.0~3.5C.4.0~4.5
(6)CoC2O4•2H2O热分解质量变化过程如图2所示.其中600℃以前是隔绝空气加热,600℃以后是在空气中加热.A、B、C均为纯净物;C点所示产物的化学式是Co2O3.
0 162413 162421 162427 162431 162437 162439 162443 162449 162451 162457 162463 162467 162469 162473 162479 162481 162487 162491 162493 162497 162499 162503 162505 162507 162508 162509 162511 162512 162513 162515 162517 162521 162523 162527 162529 162533 162539 162541 162547 162551 162553 162557 162563 162569 162571 162577 162581 162583 162589 162593 162599 162607 203614

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(2)向浸出液中加入NaClO3的离子反应方程式:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O.
(3)已知:常温下
NH3•H2O?NH4++OH- Kb=1.8×10-5
H2C2O4?H++HC2O4- Ka1=5.4×10-2
HC2O4-?H+C2O42- Ka2=5.4×10-5
则该流程中所用(NH4)2C2O4溶液的pH<7(填“>”或“<”或“=”).
(4)加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时可选用的试剂有:A.
A.蒸馏水B.自来水C.饱和的(NH4)2C2O4溶液D.稀盐酸
(5)萃取剂对金属离子的萃取率与pH的关系如右图1,萃取剂的作用是除去溶液中的Mn2+;其使用的适宜pH范围是B.
A.2.0~2.5B.3.0~3.5C.4.0~4.5
(6)CoC2O4•2H2O热分解质量变化过程如图2所示.其中600℃以前是隔绝空气加热,600℃以后是在空气中加热.A、B、C均为纯净物;C点所示产物的化学式是Co2O3.

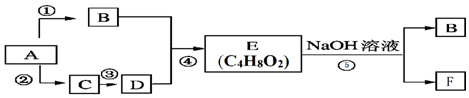

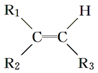 $\stackrel{氧化}{→}$
$\stackrel{氧化}{→}$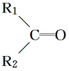 +R3COOH
+R3COOH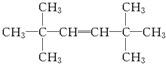 G:
G: .
.