题目内容
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 无色中性溶液中:Na+、K+、CO32-、SO42- | |
| B. | 含有大量Fe3+的溶液中:Na+、Mg2+、NO3-、I- | |
| C. | 加入铝粉后有气体放出的溶液:Fe2+、K+、NO3-、Cl- | |
| D. | 能使酚酞变红色的溶液:CO32-、Cl-、F-、K+ |
分析 A.CO32-水解显碱性;
B.离子之间发生氧化还原反应;
C.加入铝粉后有气体放出的溶液,为非氧化性酸或强碱溶液;
D.能使酚酞变红色的溶液,显碱性.
解答 解:A.CO32-水解显碱性,与中性不符,则不能大量存在,故A错误;
B.Fe3+、I-发生氧化还原反应,不能共存,故B错误;
C.加入铝粉后有气体放出的溶液,为非氧化性酸或强碱溶液,强碱溶液中不能大量存在Fe2+,酸溶液中Al或Fe2+、H+、NO3-发生氧化还原反应不生成氢气,故C错误;
D.能使酚酞变红色的溶液,显碱性,该组离子之间不反应,可大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
16.下列化学变化属于取代反应的是( )
| A. | 甲烷在空气中完全燃烧 | |
| B. | 在镍做催化剂的条件下,苯与氢气反应 | |
| C. | 乙烯通入溴水中 | |
| D. | 乙醇与乙酸制备乙酸乙酯 |
13.下列说法正确的是( )
| A. | 按系统命名法,有机物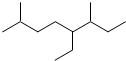 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 | |
| B. | 环己醇分子中所有的原子可能共平面 | |
| C. | 麻黄碱(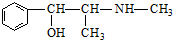 )的催化氧化产物能发生银镜反应 )的催化氧化产物能发生银镜反应 | |
| D. | 某分子式为C10H20O2的酯可发生如图所示的转化过程,则符合条件的酯的结构有4种 |
10.下列过程中,最终的白色沉淀不一定是BaSO4的是( )
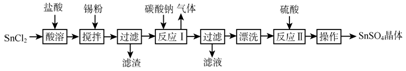
| A. | Ba(NO3)2溶液$\stackrel{通入SO_{2}}{→}$白色沉淀 | |
| B. | 无色溶液$\stackrel{稀HNO_{3}}{→}$ $\stackrel{BaCl_{2}溶液}{→}$白色沉淀 | |
| C. | Ba(NO3)2溶液$\stackrel{加过量HCl}{→}$无现象 $\stackrel{Na_{2}SO_{4}}{→}$白色沉淀 | |
| D. | Fe(NO3)2溶液$\stackrel{加过量HCl}{→}$ $\stackrel{通入SO_{2}}{→}$ $\stackrel{BaCl_{2}}{→}$白色沉淀 |
17.下列反应的离子方程式书写正确的是( )
| A. | 铁和稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| B. | 惰性电极电解熔融氯化钠:2Clˉ+2H2O$\frac{\underline{\;电解\;}}{\;}$2OHˉ+H2↑+Cl2↑ | |
| C. | 等体积等物质的度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO32-+NH4+═BaCO3↓+NH3•H2O+H2O | |
| D. | 向FeCl3溶液中滴加KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ |
14.下列关于卤族元素结构和性质的说法错误的是( )
| A. | F、Cl、Br、I原子半径依次增大 | |
| B. | F、Cl、Br、I的电子层数逐渐增多 | |
| C. | F2、Cl2、Br2、I2的氧化性逐渐减弱 | |
| D. | F-、Cl-、Br -、I-离子的还原性依次减弱 |
13.由乙烯推测丙烯(CH2=CHCH3)的结构或性质正确的是( )
| A. | 不能使酸性高锰酸钾溶液褪色 | |
| B. | 所有原子都在同一平面上 | |
| C. | 能使溴水褪色 | |
| D. | 与HCl在一定条件下能加成只得到一种产物 |