12.下列说法中错误的是( )
| A. | 根据对角线规则,铍和铝的性质具有相似性 | |
| B. | 在H3O+、NH4+和[Cu(NH3)4]2+中都存在配位键 | |
| C. | O3与SO2的结构相似 | |
| D. | P4和CH4都是正四面体分子且键角都为109°28ˊ |
11.下列说法正确的是( )
| A. | 同分异构现象只存在于有机物和无机物之间 | |
| B. | 同分异构现象不存在于无机物之间 | |
| C. | 在无机化合物和有机化合物间一定存在同分异构现象 | |
| D. | 在无机化合物和有机化合物间可能存在同分异构现象 |
10.已知氢化锂(LiH)属于离子化合物,LiH跟水反应可以放出氢气.下列叙述中正确的是( )
| A. | LiH跟水反应后的溶液显中性 | B. | LiH在化学反应中是一种强氧化剂 | ||
| C. | LiH中氢离子可以被还原成氢气 | D. | LiH中氢离子半径比锂离子半径大 |
9.在下列结构的有机化合物中①CH3-CH2-CH2-CH2-CH3
②CH3-CH2-CH2-CH2-CH2-CH3
③
④
⑤
属于同分异构体的是( )
②CH3-CH2-CH2-CH2-CH2-CH3
③

④

⑤

属于同分异构体的是( )
| A. | ①②和④ | B. | ②③和⑤ | C. | ①和② | D. | ④和③ |
8.室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.lmol.L-1的三种酸HA、HB和HD溶液,pH随NaOH溶液体积变化如图.下列说法不正确的是( )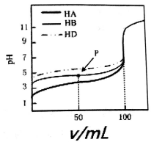

| A. | HA、HB和HD均为弱酸 | |
| B. | P点时,c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) | |
| C. | pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) | |
| D. | 三种酸溶液分别被NaOH溶液恰好完全中和后互混:c(HA)+c(HB)+c(HD)═c(OH-)-c(H+) |
7.常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,溶液的pH随溶液体积变化的曲线如图所示,则下列叙述正确的是( )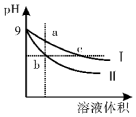

| A. | b、c两点溶液的导电能力b>c | |
| B. | 用等浓度的盐酸分别与等体积的b、c处溶液恰好完全反应,消耗盐酸体积Vb>Vc | |
| C. | c点溶液中c(H+)=c (OH-)+c(CH3COOH) | |
| D. | a、b、c三点溶液中水的电离程度a>c>b |
6.室温下,将1.000mol•L-1盐酸逐滴滴入20.00mL 1.000mol•L-1氨水中.溶液的pH和温度随加入盐酸的体积变化曲线如图所示.下列说法不正确的是( )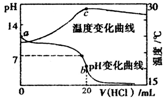

| A. | a点由水电离出的c(H+)<1.0×10-14mol•L-1 | |
| B. | b点时存在c(NH4+)+c(NH3•H2O)=c(C1-) | |
| C. | c点以后溶液温度下降的原因是盐酸的持续加入 | |
| D. | 在整个过程中可能会出现的离子浓度关系:c(NH4+)=c(C1-)>c(H+)=c(OH-) |
5.图1是硫元素在自然界的循环情况.

(1)有关叙述中不正确的是ac(填序号)
a.自然界不存在游离态的硫
b.部分硫元素由地壳到大气的过程发生了氧化反应
c.图1显示大气中的二氧化硫最终回到海洋并很快和其它矿物形成煤和石油
d.葡萄酒中含有二氧化硫可防止葡萄酒被氧化
(2)硫铁矿(FeS2)燃烧产生的SO2通过下列碘循环工艺过程既能制H2SO4,又能制H2而获得清洁能源.
①该循环工艺过程的总反应方程式为SO2+2H2O=H2+H2SO4.
②FeS2可和盐酸发生复分解反应生成一种不稳定的液态化合物,该化合物的电子式
③用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是减小生成物浓度,平衡正向移动,提高HI的分解率.
④已知下列三个反应:
a Cl(g)+H(g)═HCl(g)△H1 b Br(g)+H(g)═HBr(g)△H2 c I(g)+H(g)═HI(g)△H3
则△H1、△H2、△H3由大到小的顺序为△H3>△H2>△H1,用原子结构解释原因Cl、Br、I为同主族元素,从上至下,原子半径依次知道,非金属性依次减弱,氢化物稳定性依次减弱.
(3)工业制硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.
表是不同压强、温度时SO2的转化率情况.
工业中SO2转化为SO3通常采用400℃~500℃、压强1.0MPa,而不选择更高的10MPa.其原因是压强增大10倍,转化率几乎不变.
(4)下列事实能说明H2SO3的酸性强于H2CO3的是b
a.饱和H2SO3溶液的pH小于饱和H2CO3溶液的pH.
b.同温下,等浓度的NaHSO3和NaHCO3溶液,后者的pH值大.
c.H2SO3能使酸性高锰酸钾溶液褪色,而H2CO3不能.
d.将过量SO2气体通入NaHCO3溶液中,逸出的气体能使澄清石灰水变浑浊.
0 162348 162356 162362 162366 162372 162374 162378 162384 162386 162392 162398 162402 162404 162408 162414 162416 162422 162426 162428 162432 162434 162438 162440 162442 162443 162444 162446 162447 162448 162450 162452 162456 162458 162462 162464 162468 162474 162476 162482 162486 162488 162492 162498 162504 162506 162512 162516 162518 162524 162528 162534 162542 203614

(1)有关叙述中不正确的是ac(填序号)
a.自然界不存在游离态的硫
b.部分硫元素由地壳到大气的过程发生了氧化反应
c.图1显示大气中的二氧化硫最终回到海洋并很快和其它矿物形成煤和石油
d.葡萄酒中含有二氧化硫可防止葡萄酒被氧化
(2)硫铁矿(FeS2)燃烧产生的SO2通过下列碘循环工艺过程既能制H2SO4,又能制H2而获得清洁能源.
①该循环工艺过程的总反应方程式为SO2+2H2O=H2+H2SO4.
②FeS2可和盐酸发生复分解反应生成一种不稳定的液态化合物,该化合物的电子式

③用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是减小生成物浓度,平衡正向移动,提高HI的分解率.
④已知下列三个反应:
a Cl(g)+H(g)═HCl(g)△H1 b Br(g)+H(g)═HBr(g)△H2 c I(g)+H(g)═HI(g)△H3
则△H1、△H2、△H3由大到小的顺序为△H3>△H2>△H1,用原子结构解释原因Cl、Br、I为同主族元素,从上至下,原子半径依次知道,非金属性依次减弱,氢化物稳定性依次减弱.
(3)工业制硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.
表是不同压强、温度时SO2的转化率情况.
压强 温度℃ | 0.2Mpa | 1.0Mp | 10Mpa |
| 400 | 97.2% | 99.5% | 99.7% |
| 500 | 91.5% | 96.9% | 97.8% |
| 600 | 72.6% | 85.8% | 89.5% |
(4)下列事实能说明H2SO3的酸性强于H2CO3的是b
a.饱和H2SO3溶液的pH小于饱和H2CO3溶液的pH.
b.同温下,等浓度的NaHSO3和NaHCO3溶液,后者的pH值大.
c.H2SO3能使酸性高锰酸钾溶液褪色,而H2CO3不能.
d.将过量SO2气体通入NaHCO3溶液中,逸出的气体能使澄清石灰水变浑浊.
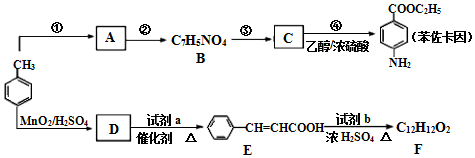

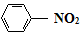 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$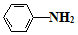 (易被氧化)
(易被氧化)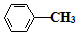 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$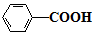
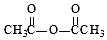 .
.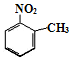 、
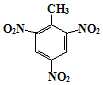
、
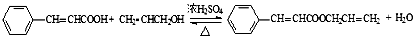 .
.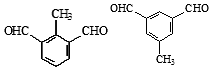 (任写一种).
(任写一种).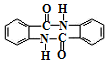 )的合成路线(无机试剂任选).
)的合成路线(无机试剂任选).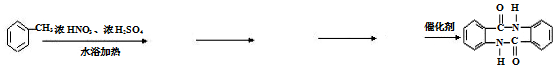
 下图是部分短周期元素化合价与原子序数的关系图,请回答下列问题:
下图是部分短周期元素化合价与原子序数的关系图,请回答下列问题: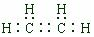 .
. ,A是一种常用的还原剂.向装有少量AgBr的试管中加入A的溶液,可观察到固体逐渐变黑,并有气泡产生,写出该反应的化学方程式4AgBr+N2H4=4Ag+N2↑+4HBr.b与c按原子数2和4构成分子B,已知A和B反应时生成无毒害物质,则该反应中氧化剂与还原剂的物质的量之比为1:2.
,A是一种常用的还原剂.向装有少量AgBr的试管中加入A的溶液,可观察到固体逐渐变黑,并有气泡产生,写出该反应的化学方程式4AgBr+N2H4=4Ag+N2↑+4HBr.b与c按原子数2和4构成分子B,已知A和B反应时生成无毒害物质,则该反应中氧化剂与还原剂的物质的量之比为1:2.