14.A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含哲同种元素.

已知:(I)A为金属单质;B为红褐色固体;E为密度最小的气体;G为浅绿色溶液.
(Ⅱ)D为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.
(Ⅲ)D能将某种氧化物氧化为F,F是含有三种元素的化合物.
请回答下列问题:
(1)上述反应中属于置换反应的是②⑤(填序号).
( 2)反应③(即D将某种氧化物氧化为F的离子方程式:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(3)D与氨水反应生成B的离子方程式:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+.
(4)实验室制取C的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
对气体C进行如下实验.已知整个反应过程中,每消耗0.1moI KI,转移的电子数约为3.612×l023个.请按照要求填空:

已知:(I)A为金属单质;B为红褐色固体;E为密度最小的气体;G为浅绿色溶液.
(Ⅱ)D为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.
(Ⅲ)D能将某种氧化物氧化为F,F是含有三种元素的化合物.
请回答下列问题:
(1)上述反应中属于置换反应的是②⑤(填序号).
( 2)反应③(即D将某种氧化物氧化为F的离子方程式:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(3)D与氨水反应生成B的离子方程式:Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+.
(4)实验室制取C的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
对气体C进行如下实验.已知整个反应过程中,每消耗0.1moI KI,转移的电子数约为3.612×l023个.请按照要求填空:
| 实验步骤 | 实验现象 | 用化学用语解释 |
| 将少量气体通入淀粉KI溶液 | 溶液最初变成蓝色 | Cl2+2I-=I2+2Cl-(用离子方程式表示) |
| 继续通入气体 | 溶液逐渐变成无色 | 5Cl2+I2+6H2O=2HIO3+10HCl(用化学方程式表示) |
13.Na2O2、Cl2和SO2均能使品红溶液褪色,下列说法正确的是( )
| A. | Na2O2和CO2反应中,Na2O2既是氧化剂又是还原剂 | |
| B. | Na2O2、Cl2、SO2使品红溶液褪色的原理相同 | |
| C. | 等物质的量的Cl2和SO2同时通入品红溶液中,品红褪色更快 | |
| D. | 在Na2O2中阴阳离子所含的电子数目相等 |
11.化学与生活、社会密切相关,下列说法不正确的是( )
| A. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| B. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于物理变化 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,分别可防止食物受潮、氧化变质 | |
| D. | 采用“静电除尘”“燃煤固硫”、“汽车尾气催化净化”可提高空气质量 |
10.表为短周期元素的一部分,请参照元素①~⑧在表中的位置,回答下列问题.
(1)元素⑦在元素周期表位置是第三周期ⅣA族.
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式).HNO3>H2CO3>H2SiO3或(H4SiO4)
(3)④、⑤、⑥的离子半径由大到小的顺序为(填元素符号)O2->Na+>Al3+.
(4)由①和④组成的元素质重比为1:8的化合物的电子式是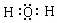 .
.
(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为.2H2O+2Al+2OH-=2AlO2-+3H2↑.
| ① | ||||||
| ② | ③ | ④ | ||||
| ⑤ | ⑥ | ⑦ | ⑧ |
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(填化学式).HNO3>H2CO3>H2SiO3或(H4SiO4)
(3)④、⑤、⑥的离子半径由大到小的顺序为(填元素符号)O2->Na+>Al3+.
(4)由①和④组成的元素质重比为1:8的化合物的电子式是
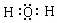 .
.(5)⑥单质与⑤的最高价氧化物的水化物反应的离子方程式为.2H2O+2Al+2OH-=2AlO2-+3H2↑.
6.化学与人类杜会生产、生活密切相关,下列说法正确的是( )
0 162135 162143 162149 162153 162159 162161 162165 162171 162173 162179 162185 162189 162191 162195 162201 162203 162209 162213 162215 162219 162221 162225 162227 162229 162230 162231 162233 162234 162235 162237 162239 162243 162245 162249 162251 162255 162261 162263 162269 162273 162275 162279 162285 162291 162293 162299 162303 162305 162311 162315 162321 162329 203614
| A. | DNOP(邻苯二甲酸二辛脂)是一种由邻苯二甲酸和正辛醇经脂化反应而得的一种酯类有机化合物,常用作增塑剂、溶剂以及气相色谱固定液,对人体无害,可用作食品添加剂 | |
| B. | 铝及其合金是电气、工业、家底广泛使用的材料,是因为铝的冶炼方法比较简单 | |
| C. | 陶瓷、砖瓦、玻璃、水泥都是硅酸盐产品 | |
| D. | 白酒标签上注有“酒精度52%Vol”字样,它表示100g该白酒中含有52g洒精 |
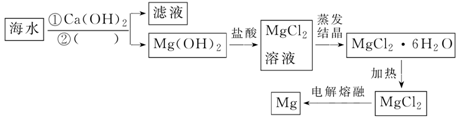
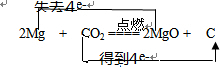 .
.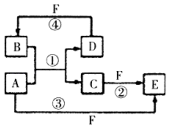 (1)短周期元素A、B、C、D、E的原子序数依次增大,A为半径最小的原子,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构,A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性,且A和E形成的化合物与A和B形成的化合物反应可产生白烟.回答下列问题:
(1)短周期元素A、B、C、D、E的原子序数依次增大,A为半径最小的原子,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构,A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性,且A和E形成的化合物与A和B形成的化合物反应可产生白烟.回答下列问题: ;
; ,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.
,反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+4NO2↑+2H2O.