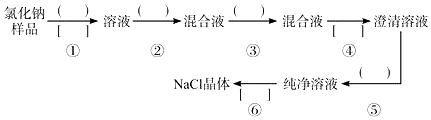
11.25℃时,下列说法不正确的是( )
| A. | 物质的量浓度相等的盐酸和氨水等体积混合,所得溶液的pH<7 | |
| B. | 物质的量浓度相等的硫酸和氨水等体积混合,所得溶液的pH<7 | |
| C. | pH=3的盐酸和pH=11的氨水等体积混合,所得溶液的pH>7 | |
| D. | pH=3的硫酸和pH=11的氨水等体积混合,所得溶液的pH<7 |
10.对于pH相等的盐酸和醋酸溶液,下列说法正确的是( )
| A. | 溶液浓度相等 | |
| B. | c(Cl-)=c(CH3COO-) | |
| C. | 等体积的两种酸,中和所需NaOH溶液的体积盐酸比醋酸多 | |
| D. | 分别加水稀释至原体积的10倍,盐酸的pH小于醋酸 |
9.下列关于有机化合物的说法正确的是( )
0 161757 161765 161771 161775 161781 161783 161787 161793 161795 161801 161807 161811 161813 161817 161823 161825 161831 161835 161837 161841 161843 161847 161849 161851 161852 161853 161855 161856 161857 161859 161861 161865 161867 161871 161873 161877 161883 161885 161891 161895 161897 161901 161907 161913 161915 161921 161925 161927 161933 161937 161943 161951 203614
| A. | 1-丁醇的结构简式可写作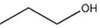 | |
| B. | 氨基酸合成多肽链属于加聚反应 | |
| C. | 分子式为C4H8O2,既含有羟基又含有醛基的同分异构体有5种 | |
| D. | 糖、油脂、蛋白质等这些人体必需的营养物质都是高分子化合物 |
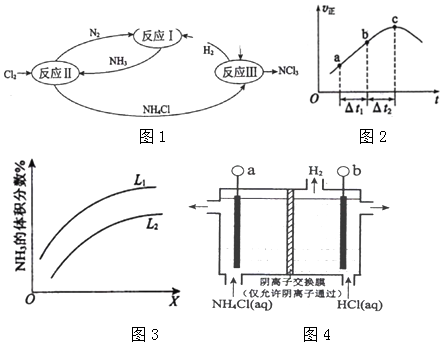
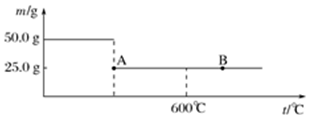
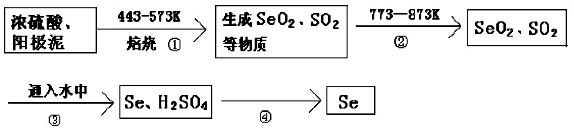


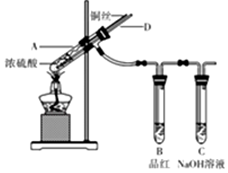 某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示:
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示: