题目内容
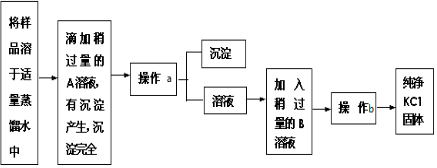
6.氯化钠样品中含有少量的杂质Na2SO4,按下列流程进行净化,请在流程中的【】中写上合适的试剂,在[]中写上实验操作名称.写出有关反应的化学方程式: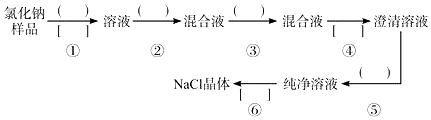
(1)操作①、②、③、⑤中所需加入试剂分别为蒸馏水、BaCl2溶液、Na2CO3溶液、稀盐酸.
(2)操作①、④、⑥的操作名称分别为溶解、过滤、蒸发结晶.
(3)写出有关的化学方程式:
第②步:Na2SO4+BaCl2═BaSO4↓+2NaCl.
第⑤步:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(4)操作④所用到的玻璃仪器有烧杯、漏斗、玻璃棒.
分析 由流程可知,氯化钠样品含有少量的Na2SO4,最后得到NaCl晶体,则①中加蒸馏水溶解,②中加BaCl2溶液,③加Na2CO3溶液,④为过滤得到澄清溶液,⑤中加稀盐酸,⑥为蒸发结晶,则流程为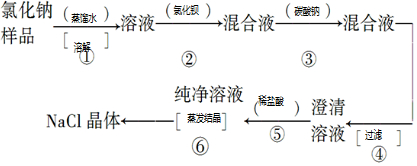 ,以此来解答.
,以此来解答.
解答 解:(1)由上述分析可知,操作①、②、③、⑤中所需加入试剂分别为蒸馏水、BaCl2溶液、Na2CO3溶液、稀盐酸,
故答案为:蒸馏水;BaCl2溶液;Na2CO3溶液;稀盐酸;
(2)由以上分析可知操作①、④、⑥的操作名称分别为溶解、过滤、蒸发结晶,故答案为:溶解;过滤;蒸发结晶;
(3)第②步中发生Na2SO4+BaCl2═BaSO4↓+2NaCl、第⑤步发生Na2CO3+2HCl═2NaCl+H2O+CO2↑,
故答案为:Na2SO4+BaCl2═BaSO4↓+2NaCl;Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(4)操作④为过滤,所用到的玻璃仪器有烧杯、漏斗、玻璃棒,故答案为:烧杯、漏斗、玻璃棒.
点评 本题考查混合物分离提纯,为高频考点,把握流程中的反应、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意碳酸钠一定在氯化钡之后,题目难度不大.

练习册系列答案
相关题目
17.对于反应2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O的说法不正确的是( )
| A. | 该反应中,KMnO4是还原剂 | |
| B. | 该反应中,C元素被氧化 | |
| C. | 通过该反应可知,氧化性:KMnO4>CO2 | |
| D. | 该反应每转移1mol电子,同时生成1molCO2 |
14.用如图装置进行实验,将液体A逐滴加入到固体B中(必要时可加热),下列叙述错误的是( )
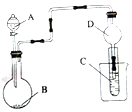

| A. | 若A为浓氨水,B为生石灰,C中盛有AlCl3溶液,则C中产生白色沉淀,白色沉淀不会消失 | |
| B. | 实验仪器D可以起到防止溶液倒吸的作用 | |
| C. | 若A为浓盐酸,B为MnO2,C中盛石蕊溶液,则C中溶液先变红后褪色 | |
| D. | 若A为浓盐酸,B为贝壳,C中盛有硅酸钠溶液,则C中出现白色沉淀可证明酸性的强弱为:碳酸>硅酸 |
11.25℃时,下列说法不正确的是( )
| A. | 物质的量浓度相等的盐酸和氨水等体积混合,所得溶液的pH<7 | |
| B. | 物质的量浓度相等的硫酸和氨水等体积混合,所得溶液的pH<7 | |
| C. | pH=3的盐酸和pH=11的氨水等体积混合,所得溶液的pH>7 | |
| D. | pH=3的硫酸和pH=11的氨水等体积混合,所得溶液的pH<7 |
16.下列有关方程式正确的是( )
| A. | 碳酸钠溶液呈碱性:CO32-+H2O?HCO3-+OH- | |
| B. | 碳酸溶液呈酸性:H2CO3?2H++CO32- | |
| C. | Cl2溶于水:Cl2+H2O?Cl-+ClO-+2H+ | |
| D. | 往有足量的碳酸镁固体的溶液中加入NaOH固体:Mg2++2OH-═Mg(OH)2(已知:Ksp(Mg(OH)2)>Ksp(MgCO3) |