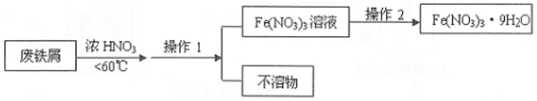
题目内容
15.概及其化合物的转化是资源利用和环境保护的重耍研究课题,下面是氮及氮的化合物的几种不同情况下的转化图1.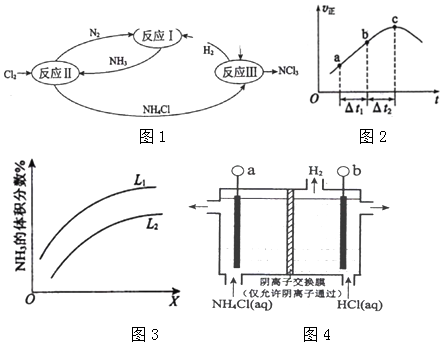
(1)已知:
2SO2(g)+O2(g)?2SO3 (g)△H=-196.6kJ•mol-1
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ•mol-1
则SO2(g)+NO2(g)?SO3(g)+NO(g)△H-41.8kJ•mol-1
(2)向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应 SO2(g)+NO(g)?SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图2所示.
反应在 c点未到(填“达到”或“未到”)平衡状态,若保持容器恒温恒容,在该容器中加入:1mol SO2(g)和lmol NO2(g),下列说法正确的是BD
A.若容器内气体密度恒定时,标志反应达到平衡状态
B.不断增加SO2的量可以提高NO2的转化率
C.待反应达平衡后继续向容器中再通入QmolSO2(g)和ImolNO2(g),则平衡将正向移动,K值也将变大
D.待反应达平衡后通入氮气,则平衡将不移动
(3)反应I:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,图3是反应I中平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强.其中L代表的是温度.(填“温度”或“压强”),判断L1、L2的大小关系并说明理由L1<L2,合成氨是放热反应升温平衡逆向进行氨气体积分数减小
(4)反应Ⅲ是利用图4所示装置电解制备NCl3 (l氯的化合价为+1),其原理是:NH4Cl+2HC1 $\frac{\underline{\;电解\;}}{\;}$NCl3+3H2↑
①a接电源的正极(填“正”或“负”).
②阳极反应式是3Cl--6e-+NH4+=NCl3+4H+.
(5)反应Ⅲ得到的NCl3可以和NaClO2制备C1O2,同时生成NH3,该反应的离子方程式是NCl3+6ClO2-+3H2O=6ClO2+NH3+3Cl-+3OH-.
分析 (1)依据盖斯定律和热化学方程式计算得到SO2(g)+NO2(g)?SO3(g)+NO(g)反应的焓变;
(2)①由题意可知一个反应前后体积不变的可逆反应,由于容器恒容,因此压强不影响反应速率,所以在本题中只考虑温度和浓度的影响.结合图象可知反应速率先增大再减小,因为只要开始反应,反应物浓度就要降低,反应速率应该降低,但此时正反应却是升高的,这说明此时温度的影响是主要的,由于容器是绝热的,因此只能是放热反应,从而导致容器内温度升高反应速率加快;
②A.保持容器恒温恒容,气体质量不变,气体体积不变,密度始终不变;
B.两种反应物增大一种会提高另一种物质的转化率;
C.平衡常数随温度变化;
D.待反应达平衡后通入氮气,总压增大分压不变,平衡不动;
(3)升高温度,平衡向吸热的方向移动;增大压强,平衡向气体体积缩小的方向移动;
(4)①阴极与电源负极相连,阳极与电源正极相连;
②阴极电极反应为氢离子得电子生成氢气,用总反应减掉阴极反应得阳极反应;
(5)反应III得到的NCl3可以和NaClO2制备 ClO2,同时生成NH3,根据氧化还原化合价升降原理,Cl元素化合价有升高和讲点,根据得失电子守恒配平反应,
故答案为:NCl3+6ClO2-+3H2O=6ClO2+NH3+3Cl-+3OH-.
解答 解:(1)①2SO2(g)+O2(g)?2SO3 (g)△H=-196.6kJ•mol-1
②2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ•mol-1
盖斯定律计算(①-②)×$\frac{1}{2}$得到,SO2(g)+NO2(g)?SO3(g)+NO(g)△H=-41.8KJ/mol,
故答案为:41.8;
(2)化学平衡状态的标志是各物质的浓度不再改变,其实质是正反应速率等于逆反应速率,c点对应的正反应速率显然还在改变,故一定未达平衡,
A.保持容器恒温恒容,气体质量不变,气体体积不变,密度始终不变,若容器内气体密度恒定时,不能说明反应达到平衡状态,故A错误;
B.不断增加SO2的量可以提高NO2的转化率,故B正确;
C.待反应达平衡后继续向容器中再通入QmolSO2(g)和ImolNO2(g),则平衡将正向移动,K值不变,故C错误;
D.待反应达平衡后通入氮气,总压增大分压不变,平衡不移动,故D正确;
故答案为:未到;BD;
(3)N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1为放热反应,若升高温度平衡逆向移动,前期的体积分数减小,与图象矛盾;若增大压强,平衡向正向移动,氨气的体积分数增大,故改变条件为压强,L为温度,压强相同时,温度升高,平衡逆向移动,氨的体积分数减小,L1<L2,
故答案为:温度;L1<L2;合成氨的反应是放热反应,压强相同时,温度升高,平衡逆向移动,氨的体积分数减小;
(4)①b极产生氢气,为阴极,与电源负极相连,a极为阳极与电源正极相连,
故答案为:正;
②阴极电极反应为氢离子得电子生成氢气,用总反应减掉阴极反应得阳极反应式,3Cl--6e-+NH4+=NCl3+4H+,
故答案为:3Cl--6e-+NH4+=NCl3+4H+;
(5)反应III得到的NCl3可以和NaClO2制备 ClO2,同时生成NH3,根据氧化还原化合价升降原理,Cl元素化合价有升高和讲点,根据得失电子守恒配平反应,
故答案为:NCl3+6ClO2-+3H2O=6ClO2+NH3+3Cl-+3OH-.
点评 本题考查了化学反应速率、化学平衡影响因素、原电池反应等知识点,主要是反应能量变化的计算,要求正确书写方程式,学生需有扎实的基础,试题难度中等.

| A. | Na2CO3溶液显碱性:CO32-+2H2O═H2CO3+2OH- | |
| B. | HS-电离的离子方程式:HS-+H2O═H3O++S2- | |
| C. | 少量氢氧化钙溶液与碳酸氢钠溶液混合,反应的离子方程式:Ca2++2HCO3-+2OH-═CaCO3+2H2O+CO32- | |
| D. | 在0.5 mol•L-1的K2Cr2O7溶液中存在如下平衡:Cr2O72-+H2O═2CrO42-+2H+,其平衡常数的表达式为$\frac{{{c^2}(CrO_4^{2-})•{c^2}({H^+})}}{{c(C{r_2}O_7^{2-})}}$ |
| A. | 相同物质的量的石墨与金刚石相比,金刚石的总能量更高 | |
| B. | 金刚石转化为石墨是放热反应,金刚石比石墨稳定 | |
| C. | 金刚石转化为石墨是吸热反应,石墨比金刚石稳定 | |
| D. | 两者互为同位素 |
| A. | 溶液浓度相等 | |
| B. | c(Cl-)=c(CH3COO-) | |
| C. | 等体积的两种酸,中和所需NaOH溶液的体积盐酸比醋酸多 | |
| D. | 分别加水稀释至原体积的10倍,盐酸的pH小于醋酸 |
| A. | C3H6和 C5H10 | B. | C3H4和 C4H6 | C. | C2H6和 C8H18 | D. | C2H6和 C3H6 |
| A. | NO2和NO | B. | NO2和CO2 | C. | N2和O2 | D. | O2和CO |
| A. | 分子式为C5H11Cl的有机物,分子中含2个甲基的同分异构体有4种 | |
| B. | 甲苯与氯气在光照下反应主要生成2,4--二氯甲苯 | |
| C. | 苯酚、甲醛通过加聚反应可制得酚醛树脂 | |
| D. | 合成顺丁橡胶( 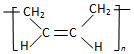 )的单体是CH3-CH=CH-CH3 )的单体是CH3-CH=CH-CH3 |
| A. | 盐酸:强电解质 | B. | 氧化铝:两性氧化物 | ||
| C. | 熔融的硫酸钠:电解质 | D. | 次氯酸:氧化性酸 |