1.实验室需配制500mL 0.4mol/L Na2SO4溶液,请你参与实验过程,并完成相关实验报告(填写表格中横线上数字序号所示内容).
| 实验原理 | m=cVM |
| 实验仪器 | 托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管 |
| 实验步骤 | (1)计算:溶质Na2SO4固体的质量为28.4g. (2)称量:用托盘天平称取所需Na2SO4固体. (3)溶解:将称好的Na2SO4固体放入烧杯中,用适量蒸馏水溶解. (4)转移、洗涤:将烧杯中的溶液冷却至室温并注入仪器①中,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也都注入仪器①中. (5)定容:将蒸馏水注入仪器至液面离刻度线1~2cm时,改用胶头滴管滴加蒸馏水至液面与刻度线相切. (6)摇匀:盖好瓶塞,反复上下颠倒,然后静置. |
| 思考与探究 | (1)实验步骤(3)、(4)中都要用到玻璃棒,其作用分别是搅拌、引流 (2)某同学在实验步骤(6)后,发现凹液面低于刻度线,该同学所配置溶液是浓度=(填“>”、“=”或“<”)0.4mol/L. |
20.常温下,某溶液中c(H+)=1×10-11mol/L,则该溶液的PH是( )
| A. | 3 | B. | 7 | C. | 8 | D. | 11 |
19.下列叙述中,不能说明醋酸是弱电解质的是( )
| A. | CH3COONa溶液显碱性 | |
| B. | CH3COOH能与氨水发生中和反应 | |
| C. | 室温下,0.1mol/L的CH3COOH溶液的PH为3 | |
| D. | 相同条件下,等浓度的醋酸溶液的导电能力比盐酸弱 |
18.下列叙述正确的是( )
| A. | 通常,同周期元素的第一电离能ⅦA族的元素最大 | |
| B. | 在同一主族中,自上而下第一电离能逐渐减小 | |
| C. | 第ⅠA、ⅡA族元素的原子,其半径越大,第一电离能越大 | |
| D. | 主族元素的原子形成单原子离子时的化合价数都和它的族序数相等 |
17.以NA表示阿佛加德罗常数,下列说法中正确的是( )
| A. | 78g过氧化钠中含2NA个O2- | |
| B. | 0.1molOH-含NA个电子 | |
| C. | 1.8g重水(D2O)中含NA个中子 | |
| D. | 标准状况下11.2L臭氧中含NA个氧原子 |
16.已知:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l);△H=-1451.6kJ•mol-1.下列叙述正确的是( )
| A. | 该反应是吸热反应 | |
| B. | 2mol甲醇所具有的能量是1451.6 kJ | |
| C. | 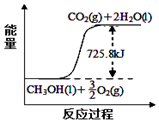 如图是CH3OH(l)燃烧反应过程的能量变化示意图 | |
| D. | 25℃、101kPa时,1 mol甲醇完全燃烧生成CO2和液态水,同时放出725.8 kJ热量 |
15.“酸雨”的形成主要是由于是( )
| A. | 煤燃烧时产生大量CO2 | B. | 煤不完全燃烧产生大量CO | ||
| C. | 煤燃烧时产生大量SO2 | D. | 工业生产中排放大量烟尘 |
13.下列关于环境问题的说法正确的是( )
| A. | 燃煤时加适量的生石灰可减少二氧化硫的排放 | |
| B. | pH在5.6~7.0之间的降水通常称为酸雨 | |
| C. | 焚烧一次性饭盒可减少白色污染 | |
| D. | 实验室可用氢氧化钠溶液除去尾气中的NO气体 |
12.酸雨的形成主要原因是( )
0 161683 161691 161697 161701 161707 161709 161713 161719 161721 161727 161733 161737 161739 161743 161749 161751 161757 161761 161763 161767 161769 161773 161775 161777 161778 161779 161781 161782 161783 161785 161787 161791 161793 161797 161799 161803 161809 161811 161817 161821 161823 161827 161833 161839 161841 161847 161851 161853 161859 161863 161869 161877 203614
| A. | 森林乱砍乱伐 | B. | 工业上大量使用含硫燃料 | ||
| C. | 大气中二氧化碳含量增多 | D. | 汽车排放出大量尾气 |