4.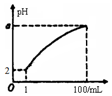 pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )
pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )
 pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )
pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )| A. | a的取值范围为2<a<4 | |
| B. | HA溶液加热时,溶液酸性增强 | |
| C. | 与pH=12的NaOH溶液等体积混合后溶液的pH=7 | |
| D. | HA溶液与NaOH溶液恰好完全反应时,c(Na+)>c(A-)>c(OH-)>c(H+) |
3.根据热化学方程S ( s )+O2 ( g )=SO2 ( g )△H=-297.23kJ/mol (反应在298K,101kPa下发生)分析下列说法不正确的是( )
| A. | 标况下,燃烧1mol S放出的热量为297.23 kJ | |
| B. | S ( g )+O2 ( g )=SO2 ( g ) 放出的热量大于297.23 kJ | |
| C. | S ( g )+O2 ( g )=SO2 ( g ) 放出的热量小于297.23 kJ | |
| D. | 形成1 mol SO2 的化学键所释放的总能量大于断裂 1 molS ( s )和 1mol O2 ( g )的化学键所吸收的总能量 |
2.将三份1mol X气体和3mol Y气体分别充入体积为2L的A,B,C三个容器中,发生反应X(g)+3Y(g)?2Z(g).2min后反应达到平衡,测得A中剩余0.4mol X,B中Y的平衡浓度为0.5mol/L,C中用Z表示的反应速率为:v(Z)=0.3mol/(L•min),则这段时间内三个容器中反应速率的大小关系为( )
| A. | B>A>C | B. | A>B=C | C. | B>A=C | D. | B>C>A |
20.下列实验装置图正确且能达到实验目的是( )
| A. | 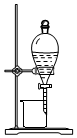 如图所示装置可从碘的CCl4溶液中分离出碘 | |
| B. | 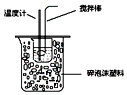 如图所示装置可用于在实验室测定中和反应的反应热 | |
| C. | 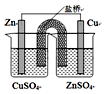 如图所示装置能构成锌铜原电池 | |
| D. | 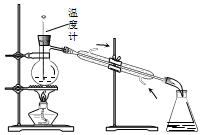 如图所示装置可用于实验室中分馏石油 |
19.含20.0g NaOH的稀溶液与稀硝酸完全反应时,放出28.7kJ的热量,表示该反应的热化学方程式正确的是( )
| A. | NaOH(aq)+HNO3(aq)=NaNO3 (aq)+H2O(l)△H=+28.7kJ•mol-1 | |
| B. | NaOH+HNO3=NaNO3+H2O△H=-28.7kJ•mol-1 | |
| C. | NaOH(aq)+HNO3 (aq)=NaNO3 (aq)+H2O(l)△H=-57.4 kJ•mol-1 | |
| D. | NaOH(aq)+HNO3 (aq)=NaNO3 (aq)+H2O(l)△H=-57.4 kJ |
17.已知某盐酸、氯化铜、氯化铁的混合溶液100mL,已知溶液中各阳离子物质的量浓度相等,氯离子总物质的量浓度为6mol•L-1,此溶液中最多可以溶解铁粉的质量为( )
0 160768 160776 160782 160786 160792 160794 160798 160804 160806 160812 160818 160822 160824 160828 160834 160836 160842 160846 160848 160852 160854 160858 160860 160862 160863 160864 160866 160867 160868 160870 160872 160876 160878 160882 160884 160888 160894 160896 160902 160906 160908 160912 160918 160924 160926 160932 160936 160938 160944 160948 160954 160962 203614
| A. | 5.6g | B. | 16.8g | C. | 11.2g | D. | 33.6g |
 +3Br2→
+3Br2→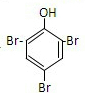 +3HBr
+3HBr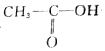 +H-O-CH2CH3$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O
+H-O-CH2CH3$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O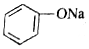 +CO2+H2O→C6H5OH+NaHCO3.
+CO2+H2O→C6H5OH+NaHCO3.