题目内容
4.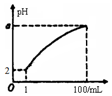 pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )
pH=2的弱酸HA溶液1mL,加水稀释到100mL,其pH与溶液体积(V)的关系如图示,下列说法不正确的是( )| A. | a的取值范围为2<a<4 | |
| B. | HA溶液加热时,溶液酸性增强 | |
| C. | 与pH=12的NaOH溶液等体积混合后溶液的pH=7 | |
| D. | HA溶液与NaOH溶液恰好完全反应时,c(Na+)>c(A-)>c(OH-)>c(H+) |
分析 A.HA为弱酸加水稀释促进电离;
B.弱酸存在电离平衡,电离过程为吸热过程,加热促进电离;
C.pH=2的弱酸HA与pH=12的NaOH溶液等体积混合后,弱酸有电离出氢离子,溶液显酸性;
D.HA溶液与NaOH溶液恰好完全反应生成NaA,溶液中A-离子水解溶液显碱性;
解答 解:A.HA为弱酸加水稀释促进电离,pH=2的弱酸HA溶液1mL,加水稀释到100mL,溶液PH大于2小于4,a的取值范围为2<a<4,故A正确;
B.HA溶液中存在电离平衡HA?H++A-,加热时促进电离平衡正向进行,氢离子浓度增大溶液酸性增强,故B正确;
C.pH=2的弱酸HA与pH=12的NaOH溶液等体积混合后,弱酸有电离出氢离子,溶液显酸性,溶液的pH<7,故C错误;
D.HA溶液与NaOH溶液恰好完全反应生成NaA,溶液中A-离子水解溶液显碱性,离子浓度大小为:c(Na+)>c(A-)>c(OH-)>c(H+),故D正确;
故选C.
点评 本题考查了酸碱反应溶液酸碱性分析、弱电解质电离平衡影响因素,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
14.常温下,下列离子在指定溶液中一定能大量共存的是( )
| A. | 某无色透明溶液中:Fe2+、Al3+、NO3-、Cl-、S2- | |
| B. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、Cl- | |
| C. | 0.1 mol•L-1的NaHCO3溶液中:K+、Na+、SO42-、CO32- | |
| D. | 加入Mg能放出H2的溶液中:Mg2+、NH4+、ClO-、K+、SO42- |
15.下列说法不正确的是( )
| A. | 用丁达尔效应可以区分Fe(OH)3胶体和FeCl3溶液 | |
| B. | 配制100g 20%的硝酸钾溶液,需要用到容量瓶 | |
| C. | 可以用萃取的方法将溴从溴水中提取出来 | |
| D. | 焰色反应实验前,应先用稀盐酸洗净铂丝,再在酒精灯上灼烧至无色 |
19.含20.0g NaOH的稀溶液与稀硝酸完全反应时,放出28.7kJ的热量,表示该反应的热化学方程式正确的是( )
| A. | NaOH(aq)+HNO3(aq)=NaNO3 (aq)+H2O(l)△H=+28.7kJ•mol-1 | |
| B. | NaOH+HNO3=NaNO3+H2O△H=-28.7kJ•mol-1 | |
| C. | NaOH(aq)+HNO3 (aq)=NaNO3 (aq)+H2O(l)△H=-57.4 kJ•mol-1 | |
| D. | NaOH(aq)+HNO3 (aq)=NaNO3 (aq)+H2O(l)△H=-57.4 kJ |
9.下列解释事实的离子方程式正确的是( )
| A. | 铁和稀硝酸反应制得浅绿色溶液:Fe+4H ++NO 3-═Fe 3++NO↑+2H 2O | |
| B. | 向Ca(ClO) 2溶液中通入过量CO 2制取次氯酸:2ClO-+H 2O+CO 2═2HClO+CO 32- | |
| C. | 向酸性KMnO 4溶液中通入SO 2:2MnO 4-+5SO 2+4OH -═2Mn 2++5SO 42-+2H 2O | |
| D. | 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ |
16.对于某些离子的检验及结论一定正确的是( )
| A. | 某物质进行焰色反应时呈现黄色,则该物质中一定含有Na+ | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,该溶液中不一定含有CO32- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
14.下列化学用语表述正确的是( )
| A. | 二氧化碳的结构式:O=C=O | B. | 氯化氢的电子式: | ||
| C. | ${\;}_{1}^{3}$H的原子结构示意图: | D. | 水的电离方程式:H2O=H++OH- |