20.下列叙述正确的是( )
| A. | NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心 | |
| B. | CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心 | |
| C. | H2O是极性分子,分子中O原子和2个H原子不在一条直线上 | |
| D. | CO2是非极性分子,分子中C原子和2个O原子不在一条直线上 |
19.下列关于乙烯(CH2=CH2)的说法正确的( )
| A. | 乙烯分子有1个δ键,1个π键 | |
| B. | 乙烯分子中2个碳原子都是sp3杂化 | |
| C. | 乙烯分子存在非极性键 | |
| D. | 乙烯分子中所有原子都在同一直线上 |
16.氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸,在空气中迅速被氧化成绿色,见光分解变成褐色;如图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程如下:
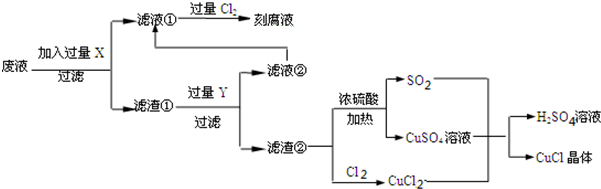
根据以上信息回答下列问题:
(1)该生产过程可以与氯碱工业、硫酸工业生产相结合,现代氯碱工业的装置名称是离子交换膜电解槽_此空删去.
(2)流程中的X是Fe,Y是HCl (均填化学式).
(3)产生CuCl的化学方程式为CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(4)为了提髙CuCl产品的质量,采用抽滤或者减压过滤法快速过滤,析出的CuCl晶体不用水洗涤而用无水乙醇洗涤,其目的是CuCl微溶于水、不溶于乙醇,用乙醇洗涤可减少产品CuCl的损失,生产过程中控制溶液的pH不能过大的原因是溶液pH大会促进CuCl的水解.
(5)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是防止CuCl的氧化和见光分解.
(6)氯化亚铜的定量分析:
①称取样品0.25g 置于预先放入10mL过量的FeCl3溶液250mL的锥形瓶中,不断摇动;
②待样品溶解后,加水50mL、邻菲罗啉指示剂2滴;
③立即用0.10mol•L-1硫酸铈Ce(SO4)2标准溶液滴至绿色出现为终点.同时做空白试验一次.已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+,如此再重复二次实验得到以下数据:
(说明:空白试验指在不加试样的情况下按试样分析规程在同样的操作条件下进行的分析,所得结果的数值为空白值)
④数据处理:计算得该工业CuCl的纯度为95%.(平行实验结果相差不能超过0.3%)

根据以上信息回答下列问题:
(1)该生产过程可以与氯碱工业、硫酸工业生产相结合,现代氯碱工业的装置名称是离子交换膜电解槽_此空删去.
(2)流程中的X是Fe,Y是HCl (均填化学式).
(3)产生CuCl的化学方程式为CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(4)为了提髙CuCl产品的质量,采用抽滤或者减压过滤法快速过滤,析出的CuCl晶体不用水洗涤而用无水乙醇洗涤,其目的是CuCl微溶于水、不溶于乙醇,用乙醇洗涤可减少产品CuCl的损失,生产过程中控制溶液的pH不能过大的原因是溶液pH大会促进CuCl的水解.
(5)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是防止CuCl的氧化和见光分解.
(6)氯化亚铜的定量分析:
①称取样品0.25g 置于预先放入10mL过量的FeCl3溶液250mL的锥形瓶中,不断摇动;
②待样品溶解后,加水50mL、邻菲罗啉指示剂2滴;
③立即用0.10mol•L-1硫酸铈Ce(SO4)2标准溶液滴至绿色出现为终点.同时做空白试验一次.已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+,如此再重复二次实验得到以下数据:
| 1 | 2 | 3 | |
| 空白试验消耗硫酸铈标准溶液的体积(ml) | 0.75 | 0.50 | 0.80 |
| 0.25克样品消耗硫酸铈标准溶液的体积(ml) | 24.65 | 24.75 | 24.70 |
④数据处理:计算得该工业CuCl的纯度为95%.(平行实验结果相差不能超过0.3%)
15.工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如图1:
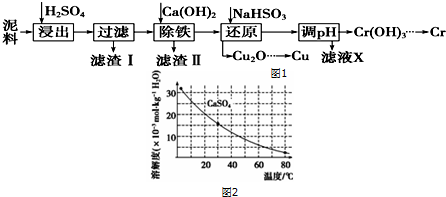
已知部分物质沉淀的pH如下表,CaSO4的溶解度曲线如图2:
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有CuSO4.
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH范围是3.2~4.3,检验Fe3+已经除尽的操作是取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除;
②将浊液加热到80℃,趁热过滤
(3)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式:2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是产生SO2污染环境.
(4)当离子浓度小于或等于1×10-5mol•L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥4.0×10-9 mol•L-1.[已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{63}$≈4.0].

已知部分物质沉淀的pH如下表,CaSO4的溶解度曲线如图2:
| 物质 | Fe3+ | Cu2+ | Cr3+ |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:
①加入石灰乳调节pH范围是3.2~4.3,检验Fe3+已经除尽的操作是取适量滤液,加KSCN溶液,若不变红,则说明Fe3+已除;
②将浊液加热到80℃,趁热过滤
(3)写出还原步骤中加入NaHSO3生成Cu2O固体反应的离子方程式:2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是产生SO2污染环境.
(4)当离子浓度小于或等于1×10-5mol•L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥4.0×10-9 mol•L-1.[已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{63}$≈4.0].
14.为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格.
供选择的化学试剂及实验方法A.将气体通入盛有NaOH溶液的洗气瓶B.取样,滴加KSCN溶液C.取样,滴加酚酞试液D.取样,灼烧.
| 实验 目 的 | 试剂及方法 |
| 鉴别丝绸和棉布 | |
| 除去CO中混有少量CO2 | |
| 证明Na2CO3溶液呈碱性 | |
| 检验溶液中是否含Fe3+ |
13.下列可以一次性鉴别氯化钾、盐酸、氢氧化钠三种溶液的试剂是( )
| A. | 紫色石蕊试液 | B. | AgNO3溶液 | C. | Na2CO3溶液 | D. | BaCl2溶液 |
12.下列实验操作正确的是( )
| A. | 用向上排空气法收集氢气 | |
| B. | 往燃着的酒精灯中添加酒精 | |
| C. | 用丁达尔现象鉴别胶体和溶液 | |
| D. | 稀释浓硫酸时,将水沿器壁慢慢注入酸中 |
11.下列不属于氧化还原反应的是( )
0 156151 156159 156165 156169 156175 156177 156181 156187 156189 156195 156201 156205 156207 156211 156217 156219 156225 156229 156231 156235 156237 156241 156243 156245 156246 156247 156249 156250 156251 156253 156255 156259 156261 156265 156267 156271 156277 156279 156285 156289 156291 156295 156301 156307 156309 156315 156319 156321 156327 156331 156337 156345 203614
| A. | S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | Fe(OH)3+3HCl═FeCl3+3H2O | ||
| C. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | D. | 4HNO3(浓)$\frac{\underline{\;光照\;}}{\;}$4NO2↑+O2↑+2H2O |
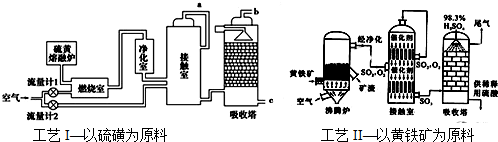
 KMnO4是锰的重要化合物,它是一种良好的氧化剂,用来漂白毛、棉和丝,或使油类脱色.其制备方法如下:
KMnO4是锰的重要化合物,它是一种良好的氧化剂,用来漂白毛、棉和丝,或使油类脱色.其制备方法如下: 2KMnO4+2KOH+H2↑.在整个制备流程中可循环利用的物质是氢氧化钾(写名称).
2KMnO4+2KOH+H2↑.在整个制备流程中可循环利用的物质是氢氧化钾(写名称).