题目内容
19.下列关于乙烯(CH2=CH2)的说法正确的( )| A. | 乙烯分子有1个δ键,1个π键 | |
| B. | 乙烯分子中2个碳原子都是sp3杂化 | |
| C. | 乙烯分子存在非极性键 | |
| D. | 乙烯分子中所有原子都在同一直线上 |
分析 A.共价单键是σ 键,共价双键中一个是σ 键一个是π键;
B.根据价层电子对互斥理论确定杂化方式;
C.同种非金属元素之间存在非极性共价键,不同非金属元素之间存在极性共价键;
D.乙烯分子的空间结构为平面方形.
解答 解:A.共价单键是σ 键,共价双键中一个是σ 键一个是π键,所以乙烯中有5个σ 键,1个π 键,故A错误;
B.乙烯分子中2个碳原子的价层电子对数为3,所以碳碳双键两端的碳原子采用sp2杂化,故B错误;
C.同种非金属元素之间存在非极性共价键,不同非金属元素之间存在极性共价键,所以分子存在非极性键,故C正确;
D.乙烯分子的空间结构为平面方形,所以4个H原子在同一平面上,故D错误;
故选B.
点评 本题考查了原子的杂化方式、分子的空间构型、极性键和非极性键的判断等知识点,利用知识迁移的方法进行分析解答,难度不大.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
10.工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用来生产Zn(NO3)2•6H2O晶体,其工艺流程为:
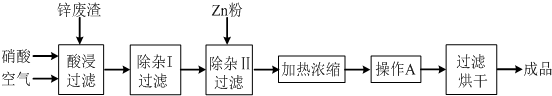
有关氢氧化物开始沉淀和沉淀完全的pH如表:
(1)在“酸浸”步骤中,为提高锌的浸出速率,除通入空气“搅拌”外,还可采取的措施是适当升高反应温度(或增大硝酸浓度、将锌废渣粉碎等).(至少写出一个措施)
(2)上述工艺流程中多处涉及“过滤”,过滤时洗涤沉淀的操作是沿着玻璃棒向过滤器注入蒸馏水浸没沉淀,水自然流下,重复2~3次.
(3)在“除杂I”步骤中,需再加入适量H2O2溶液,H2O2与Fe2+反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4.调节pH所用X可以选用AB.
A.ZnO B.ZnCO3 C.H2SO4 D.HNO3
检验Fe3+是否沉淀完全的实验操作是静置片刻,取少量上层清液,滴加KSCN溶液,若不出现血红色,表明Fe3+沉淀完全.
(4)加入Zn粉的作用是除去溶液中的Cu2+.“操作A”的名称是冷却结晶.

有关氢氧化物开始沉淀和沉淀完全的pH如表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 5.4 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.0 |
(2)上述工艺流程中多处涉及“过滤”,过滤时洗涤沉淀的操作是沿着玻璃棒向过滤器注入蒸馏水浸没沉淀,水自然流下,重复2~3次.
(3)在“除杂I”步骤中,需再加入适量H2O2溶液,H2O2与Fe2+反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4.调节pH所用X可以选用AB.
A.ZnO B.ZnCO3 C.H2SO4 D.HNO3
检验Fe3+是否沉淀完全的实验操作是静置片刻,取少量上层清液,滴加KSCN溶液,若不出现血红色,表明Fe3+沉淀完全.
(4)加入Zn粉的作用是除去溶液中的Cu2+.“操作A”的名称是冷却结晶.
7.NA为阿伏加德罗常数,下列物质所含分子数最少的是( )
| A. | 2 mol N2 | B. | 含NA个分子的Cl2 | ||
| C. | 标准状况下11.2 L的CH4 | D. | 6 g H2 (H2摩尔质量为2 g•mol-1) |
14.为达到下表中的实验目的,请选择合适的试剂及实验方法,将其标号填入对应的空格.
供选择的化学试剂及实验方法A.将气体通入盛有NaOH溶液的洗气瓶B.取样,滴加KSCN溶液C.取样,滴加酚酞试液D.取样,灼烧.
| 实验 目 的 | 试剂及方法 |
| 鉴别丝绸和棉布 | |
| 除去CO中混有少量CO2 | |
| 证明Na2CO3溶液呈碱性 | |
| 检验溶液中是否含Fe3+ |
4.一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量是14.4g,若其中水的质量是7.2g,则CO的质量是( )
| A. | 2.8 g | B. | 4.4 g | ||
| C. | 5.6 g | D. | 在2.8 g和5.6 g之间 |
11.下列关于烷烃的叙述中,正确的是( )
①在烷烃分子中,所有的化学键都是单键;
②烷烃中除甲烷外,很多都能使高锰酸钾溶液的紫色褪去;
③分子通式为CnH2n+2的烃不一定是烷烃;
④所有的烷烃在光照条件下都能与氯气发生取代反应;
⑤光照条件下,乙烷通入氯水中,可使氯水褪色.
①在烷烃分子中,所有的化学键都是单键;
②烷烃中除甲烷外,很多都能使高锰酸钾溶液的紫色褪去;
③分子通式为CnH2n+2的烃不一定是烷烃;
④所有的烷烃在光照条件下都能与氯气发生取代反应;
⑤光照条件下,乙烷通入氯水中,可使氯水褪色.
| A. | ①③⑤ | B. | ②③ | C. | ①④ | D. | ①②④ |
8.下列有关如图所示原电池装置描述正确的是( )
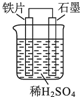

| A. | 石墨电极作负极 | |
| B. | 铁片上的反应:Fe-2e-=Fe2+ | |
| C. | 铁电极附近溶液中氢离子浓度增大 | |
| D. | 电子由石墨电极通过导线流向铁电极 |
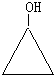
9.根据系统命名法,对烷烃 的命名正确的是( )
的命名正确的是( )
 的命名正确的是( )
的命名正确的是( )| A. | 2,4二甲基2乙基己烷 | B. | 3,5,5三甲基庚烷 | ||
| C. | 3,3,5三甲基庚烷 | D. | 3,3,5三甲基-庚烷 |
 .
.