题目内容
16.氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸,在空气中迅速被氧化成绿色,见光分解变成褐色;如图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程如下: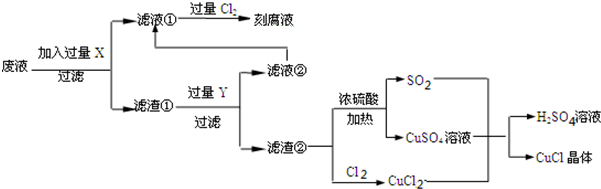
根据以上信息回答下列问题:
(1)该生产过程可以与氯碱工业、硫酸工业生产相结合,现代氯碱工业的装置名称是离子交换膜电解槽_此空删去.
(2)流程中的X是Fe,Y是HCl (均填化学式).
(3)产生CuCl的化学方程式为CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(4)为了提髙CuCl产品的质量,采用抽滤或者减压过滤法快速过滤,析出的CuCl晶体不用水洗涤而用无水乙醇洗涤,其目的是CuCl微溶于水、不溶于乙醇,用乙醇洗涤可减少产品CuCl的损失,生产过程中控制溶液的pH不能过大的原因是溶液pH大会促进CuCl的水解.
(5)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是防止CuCl的氧化和见光分解.
(6)氯化亚铜的定量分析:
①称取样品0.25g 置于预先放入10mL过量的FeCl3溶液250mL的锥形瓶中,不断摇动;
②待样品溶解后,加水50mL、邻菲罗啉指示剂2滴;
③立即用0.10mol•L-1硫酸铈Ce(SO4)2标准溶液滴至绿色出现为终点.同时做空白试验一次.已知:CuCl+FeCl3=CuCl2+FeCl2 Fe2++Ce4+=Fe3++Ce3+,如此再重复二次实验得到以下数据:
| 1 | 2 | 3 | |
| 空白试验消耗硫酸铈标准溶液的体积(ml) | 0.75 | 0.50 | 0.80 |
| 0.25克样品消耗硫酸铈标准溶液的体积(ml) | 24.65 | 24.75 | 24.70 |
④数据处理:计算得该工业CuCl的纯度为95%.(平行实验结果相差不能超过0.3%)
分析 要利用制作印刷电路的废液制备CuCl,首先应制备并分离出Cu,向工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)加入过量的Fe粉,Fe3+与Fe粉反应转化为Fe2+,Cu2+与Fe反应生成Cu,然后过滤,滤渣为过量的Fe和生成的Cu,依据Cu与Fe活泼性,将滤渣溶于盐酸,Cu与盐酸不反应,过滤得到滤渣即为Cu,然后Cu与浓硫酸反应生成CuSO4和SO2,Cu与Cl2反应生成CuCl2,CuSO4、SO2、CuCl2反应生成CuCl;
(1)氯碱工业的装置是离子交换膜电解槽;
(2)印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)加入铁,三价铁离子能够原铁反应生成二价铁离子,铜离子能够与铁反应生成铜;过滤后滤渣中含有铜和铁,依据铜和铁的活泼性,加入盐酸分离二者;
(3)依据图示可知:CuCl2、CuSO4、SO2、H2O反应生成H2SO4、CuCl,依据得失电子守恒配平方程式;
(4)抽滤或者减压过滤可以快速过滤,CuCl是一种白色粉末,微溶于水、不溶于乙醇及稀硫酸,乙醇洗涤可以减少CuCl的损失,生产过程中调节溶液的pH不能过大是防止其水解生成沉淀;
(5)依据氯化亚铜具有还原性,易被氧化而变质,具有见光分解的性质解答;
(6)依据方程式中各反应物量之间的关系计算CuCl的纯度.
解答 解:要利用制作印刷电路的废液制备CuCl,首先应制备并分离出Cu,向工业上以制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)加入过量的Fe粉,Fe3+与Fe粉反应转化为Fe2+,Cu2+与Fe反应生成Cu,然后过滤,滤渣为过量的Fe和生成的Cu,依据Cu与Fe活泼性,将滤渣溶于盐酸,Cu与盐酸不反应,过滤得到滤渣即为Cu,然后Cu与浓硫酸反应生成CuSO4和SO2,Cu与Cl2反应生成CuCl2,CuSO4、SO2、CuCl2反应生成CuCl;
(1)氯碱工业的装置是离子交换膜电解槽,
故答案为:离子交换膜电解槽;
(2)印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)加入铁,三价铁离子能够原铁反应生成二价铁离子,铜离子能够与铁反应生成铜,过滤后滤渣中含有铜和铁,加入盐酸,铁与盐酸反应生成氯化亚铁,铜与盐酸不反应,将铜分离出来,
故答案为:Fe;HCl;
(3)依据图示可知:CuCl2、CuSO4、SO2、H2O反应生成H2SO4、CuCl,产生CuCl的化学方程式依据得失电子守恒得到:CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4,
故答案为:CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4;
(4)生产中为了提高CuCl产品的质量,采用抽滤或者减压过滤法快速过滤,析出的CuCl晶体不用水而用无水乙醇洗涤的目的是:CuCl微溶于水、不溶于乙醇,用乙醇洗涤可减少CuCl的损失,生产过程中调节溶液的pH不能过大的原因是防止CuCl水解;
故答案为:抽滤或者减压过滤;CuCl微溶于水、不溶于乙醇,用乙醇洗涤可减少产品CuCl的损失;溶液pH大会促进CuCl的水解;
(5)氯化亚铜具有还原性,易被氧化而变质,具有见光分解,所以生产中应防止CuCl的氧化和见光分解,减少产品CuCl的损失,
故答案为:防止CuCl的氧化和见光分解;
(6)根据题目中所给数据及平行实验结果相差不能超过0.3%,滴定0.25g样品消耗硫酸铈标准溶液的平均体积是23.9ml,结合方程式可知:CuCl+FeCl3═CuCl2+FeCl2,CuCl的纯度为$\frac{23.9×1{0}^{-3}L×0.1mol/L×99.5g/mol}{0.25g}$×100%=95%,
故答案为:95%.
点评 本题考查物质制备,为高频考点,涉及物质分离、物质制备、氧化还原反应、元素化合物性质等知识点,正确获取题干信息并灵活运用信息解答问题是解本题关键,注意CuCl性质特点,题目难度中等.

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案| A. | 温室效应 | B. | 臭氧空洞 | C. | 酸雨 | D. | 光化学烟雾 |
| A. | S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | Fe(OH)3+3HCl═FeCl3+3H2O | ||
| C. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | D. | 4HNO3(浓)$\frac{\underline{\;光照\;}}{\;}$4NO2↑+O2↑+2H2O |
| A. | 9种 | B. | 11种 | C. | 13种 | D. | 15种 |
| A. | 同周期元素中,0族元素的原子半径最小 | |
| B. | 现已发现的ⅡA族元素的单质在常温常压下都是固体 | |
| C. | ⅦA族元素的原子,其半径越大,越容易得到电子 | |
| D. | 所有的主族元素的简单离子所带电荷与其族序数相等 |
| A. |  | B. |  | C. |  | D. |  |


