9.反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率-v(X)(反应物的消耗速率或产物的生成速率)可表示为( )
| A. | $\overline{v}$(NH3)=0.01 mol/(L•s) | B. | $\overline{v}$(O2)=0.00l0 mol/(L•s) | ||
| C. | $\overline{v}$(NO)=0.00l0 mol/(L•s) | D. | $\overline{v}$(H2O)=0.045 mol/(L•s) |
8.在密闭容器中,一定量混合气体发生下列反应:aA(g)+bB(g)?cC(g)+dD(g),达到平衡后,测得C气体的浓度为0.5mol/L.恒温下,将密闭容器的体积缩小为$\frac{1}{2}$,再达平衡时,测得C气体的浓度为0.9mol/L.则下列叙述正确的是( )
| A. | C的体积分数增大 | B. | 平衡向右移动 | C. | B的转化率提高 | D. | a+b<c+d |
7.用右图所示装置模拟电解原理在工业生产上的应用.下列说法正确的是( )
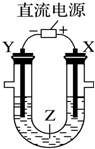

| A. | 氯碱工业中,X电极上反应式是4OH--4e-═2H2O+O2↑ | |
| B. | 电解精炼铜时,Z溶液中的铜离子浓度不变 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 电解水制氢气时,Z可以是稀硫酸溶液 |
6.一定温度下,在体积为10L的密闭容器中,3molX和1molY进行应:2X(g)+Y(g)?Z(g),经2min达到平衡,生成0.6mol Z,下列说法正确的是( )
0 154258 154266 154272 154276 154282 154284 154288 154294 154296 154302 154308 154312 154314 154318 154324 154326 154332 154336 154338 154342 154344 154348 154350 154352 154353 154354 154356 154357 154358 154360 154362 154366 154368 154372 154374 154378 154384 154386 154392 154396 154398 154402 154408 154414 154416 154422 154426 154428 154434 154438 154444 154452 203614
| A. | 以X浓度变化表示的反应速率为0.01 mol/(L•s) | |
| B. | 将容器体积变为20L,Z的平衡浓度为原来的1/2 | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H<0 |
 已知水溶液中CrO42-(黄色)和 Cr2O72-(橙色)间存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O△H<0
已知水溶液中CrO42-(黄色)和 Cr2O72-(橙色)间存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O△H<0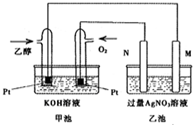 在298K时,1mol C2H5OH在氧气中完全燃烧生成二氧化碳和液态水放出热量1366.8kJ.
在298K时,1mol C2H5OH在氧气中完全燃烧生成二氧化碳和液态水放出热量1366.8kJ. 铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题:
铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题: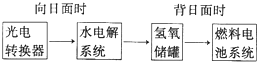
 金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速.完成下列填空:
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速.完成下列填空: