题目内容
10.“神舟七号”成功登天标志着我国的航天事业进入了新的篇章.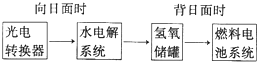
(1)某空间站局部能量转化系统如图所示,其中燃料电池采用KOH溶液为电解液,燃料电池放电时的负极反应式为H2-2e-+2OH-=H2O.如果某段时间内氢氧储罐中共收集到33.6L(已折算成标况)气体,则该段时间内水电解系统中转移电子的物质的量为2mol.
(2)在载人航天器的生态系统中,不仅要求分离出CO2,还要求提供充足的O2.某种电化学装置可实现转化2CO2═2CO+O2,CO可用作燃料.已知该反应的阳极反应式为4OH--4e-═O2↑+2H2O,则阴极反应式为CO2+2e-+H2O=CO+2OH-.
分析 (1)碱性氢氧燃料电池中,负极上氢气失电子和氢氧根离子反应生成水;根据生成气体和转移电子之间的关系式计算;
(2)该电解池中,阴极上二氧化碳得电子和水反应生成CO和氢氧根离子.
解答 解:(1)碱性氢氧燃料电池中,负极上氢气失电子和氢氧根离子反应生成水,电极反应式为H2-2e-+2OH-=H2O;电解水生成氢气和氧气的体积之比为2:1,则混合气体中生成氧气体积=$\frac{1}{3}×33.6L$=11.2L,转移电子物质的量=$\frac{11.2L}{22.4L/mol}×4$=2mol;
故答案为:H2-2e-+2OH-=H2O;2;
(2)该电解池中,阴极上二氧化碳得电子和水反应生成CO和氢氧根离子,电极反应式为 CO2+2e-+H2O=CO+2OH-,
故答案为:CO2+2e-+H2O=CO+2OH-.
点评 本题以化学电源新型电池为载体考查电极反应式的书写,为高频考点,明确各个电极上发生的反应是解本题关键,注意结合电解质溶液酸碱性书写电极反应式,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
20.在pH=1的无色透明溶液中能大量共存的离子组是( )
| A. | Al3+ Ag+ NO3- Cl- | B. | Mg2+NH4+ NO3- I- | ||
| C. | Ba2+K+ S2- Cl- | D. | Zn2+ Na+ NO3- SO42- |
1.下列关于乙醇和乙酸的说法错误的是( )
| A. | 乙醇和乙酸都是常用调味品的主要成分 | |
| B. | 相同条件下,与金属钠反应的速率,乙醇比乙酸慢 | |
| C. | 乙醇可由乙烯与水发生加成反应制得,乙酸可由乙醇氧化制得 | |
| D. | 乙醇和乙酸之间能发生酯化反应,酯化反应的逆反应为皂化反应 |
18.化学与社会、生活密切相关,下列说法正确的是( )
| A. | 纯银制品在空气中久置变黑,是因为发生了电化学腐蚀 | |
| B. | 氨常用作制冷剂,是因为其沸点极低,易液化 | |
| C. | 酸雨样品露天放置一段时间,酸性增强,是由于雨水所含成分被氧化 | |
| D. | 明矾具有强氧化性,可用作净水剂 |
15.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 盐卤可用于制作豆腐 | |
| B. | 从海水中提取物质都要通过化学反应才能实现 | |
| C. | 煤经过气化和液化等物理变化可转化为清洁燃料 | |
| D. | 制作航天服的聚醋纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
3.为了测定酸碱反应的中和热,计算时至少需要的数据是
①酸的浓度和体积;②碱的浓度和体积;③比热容;④反应后溶液的质量;⑤生成水的物质的量;⑥反应前后的温度变化;⑦操作所需时间;( )
①酸的浓度和体积;②碱的浓度和体积;③比热容;④反应后溶液的质量;⑤生成水的物质的量;⑥反应前后的温度变化;⑦操作所需时间;( )
| A. | ③④⑤⑥ | B. | ①③④⑤ | C. | ①②③⑥⑦ | D. | ①②③④⑤⑥ |
4.下图所示的实验操作,不能达到相应目的是( )
| A. | 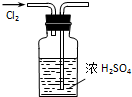 干燥Cl2 | B. | 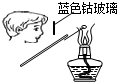 检验K2CO3中的K+ | ||
| C. | 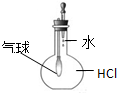 证明HCl极易溶于水 | D. |  实验室制氨气 |
 金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速.完成下列填空:
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用,利用铝热反应完成钢轨的焊接非常方便迅速.完成下列填空: