题目内容
6.一定温度下,在体积为10L的密闭容器中,3molX和1molY进行应:2X(g)+Y(g)?Z(g),经2min达到平衡,生成0.6mol Z,下列说法正确的是( )| A. | 以X浓度变化表示的反应速率为0.01 mol/(L•s) | |
| B. | 将容器体积变为20L,Z的平衡浓度为原来的1/2 | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H<0 |
分析 A.根据v=$\frac{△c}{△t}$计算v(Z),利用化学反应速率之比等于化学质量数之比计算反应速率v(X);
B.体积变为20L,体系的压强减小,平衡向逆反应方向移动;
C.增大压强平衡向正反应方向移动,反应物Y的转化率增大;
D.根据升高温度平衡向逆反应方向移动判断反应热.
解答 解:A.经2min达到平衡,生成0.6molZ,则Z的反应速率v(Z)=$\frac{\frac{0.6mol}{10L}}{120s}$=0.0005mol/(L•s),根据化学反应速率之比等于化学质量数之比,由方程式可知,v(X)=2v(Z)=2×0.0005mol/(L•s)=0.00lmol/(L•s),故A错误;
B.反应前后气体的化学计量数之和不相等,体积变为20L,体系的压强减小,平衡向逆反应方向移动,Z的平衡浓度小于原来的$\frac{1}{2}$,故B错误;
C.增大压强平衡向正反应方向移动,反应物Y的转化率增大,故C错误;
D.升高温度,X的体积分数增大,说明升高温度平衡向逆反应方向移动,则正反应的△H<0,故D正确;
故选D.
点评 本题考查化学平衡的计算,题目难度中等,明确化学平衡及其影响因素为解答关键,注意反应速率的概念及表达式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
16.只用一种试剂就能鉴别BaCl2、NH4Cl、Na2SO4、(NH4)2SO4四种溶液,此试剂是( )
| A. | HCl | B. | NaOH | C. | Ba(OH)2 | D. | Na2CO3 |
14.五种短周期元素的某些性质如表所示.下列说法正确的是( )
| 元素代号 | X | Y | Z | W | Q |
| 原子半径(nm) | 0.073 | 0.077 | 0.099 | 0.102 | 0.118 |
| 主要化合价 | -2 | +4、-4 | -1 | +6、-2 | +3 |
| A. | 单质沸点:W>Q>Z | |
| B. | X、Y、W三种元素两两之间均能以共价键形成AB2型的化合物 | |
| C. | Z的含氧酸的酸性一定大于W的含氧酸的酸性 | |
| D. | W与Q形成的常见化合物可以稳定存在于水溶液中 |
1.能正确表示下列反应的离子方程式是( )
| A. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O | |
| B. | 向次氯酸钙溶液通入SO2:Ca2++2C1O-+H2O+SO2═CaSO3↓+2HC1O | |
| C. | 氢氧化钙溶液气碳酸氢镁溶液反应:Ca2++OH-+HCO3 -═CaCO3↓+H2O | |
| D. | 硫酸亚铁的酸性溶液中加入H2O2溶液:Fe 2++H2O2+2H+═Fe 3++2H2O |
18.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某有机物与溴的四氯化碳 溶液混合 | 溶液褪色 | 该有机物中必定含有 碳碳双键 |
| B | 向亚硫酸钠溶液中滴加硝酸 钡和稀硝酸 | 产生白色沉淀 | 亚硫酸钠溶液己变质 |
| C | 向酸性高锰酸钾溶液中滴加 双氧水 | 紫色褪去,产生气泡 | H202具有还原性 |
| D | 向油脂皂化反应后的溶液中 滴入酚酞 | 溶液不变红 | 油脂己经完全皂化 |
| A. | A | B. | B | C. | C | D. | D |
15.下列有关物质分离的说法合理的是( )
| A. | 除去KNO3中少量NaCl,将混合物制成热的饱和溶液,冷却结晶,过滤 | |
| B. | 除去氯化钙溶液中的氯化铁杂质,加生石灰调节溶液的pH为3.7,再过滤 | |
| C. | 除去乙烷中混有的少量乙烯,将混合气体通入足量酸性KMnO4溶液中 | |
| D. | 加热法除去Ca(0H)2固体中混有的NH4Cl固体. |
 (R、R′、R〞表示氢、烷基或芳基)合成五元环有机化合物J 的路线如下:
(R、R′、R〞表示氢、烷基或芳基)合成五元环有机化合物J 的路线如下:
 ,它的分子子中有3种不同类型的官能团,它是J的同分异构体;
,它的分子子中有3种不同类型的官能团,它是J的同分异构体; ;
; +H2O;E的核磁共振氢谱中应该具有6组峰.
+H2O;E的核磁共振氢谱中应该具有6组峰. .
. 铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题:
铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题: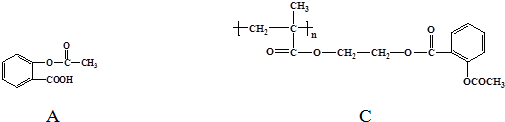
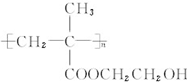 .
.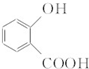 和CH3COOH(写结构简式).
和CH3COOH(写结构简式).