17.某有机物的结构简式为HO-CH2CH=CHCH2-COOH.下列说法不正确的是( )
| A. | 它能与Na、NaOH、NaHC03等物质反应 | B. | 它能发生酯化、氧化、加成等反应 | ||
| C. | 该有机物分子式为C5H8O3 | D. | 它是乙酸也是乙醇的同系物 |
16.下列说法正确的是( )
| A. | 物质发生化学反应时必然伴随着能量变化 | |
| B. | 金属铜导电,故金属铜是电解质 | |
| C. | 自发反应都是熵增大的反应 | |
| D. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
15.下列分子的立体构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH2=CH2③苯 ④CH≡CH ⑤NH3 ⑥CH4.
①BF3 ②CH2=CH2③苯 ④CH≡CH ⑤NH3 ⑥CH4.
| A. | ①②③ | B. | ①⑤⑥ | C. | ②③④ | D. | ③⑤⑥ |
14.设NA为可伏加德罗常数的值,则下列说法正确的是( )
| A. | 标准状况下,4.48LCH3Cl中含有的原子数为NA | |
| B. | 常温常压下,14 g N2含有的核外电子数为5NA | |
| C. | 10L PH=1的硫酸中含有的氢离子数为2 NA | |
| D. | 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数为2NA |
12.下列离子方程式书写正确的是( )
| A. | 用醋酸除水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 向次氯酸钙溶液中通入少量SO2:Ca2++2ClO-+H2O+SO2═CaSO3↓+2HClO | |
| C. | 碘化亚铁溶液中通入少量氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 硝酸亚铁溶液中滴加稀硫酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
11.下列说法正确的是( )
| A. | 放热反应在任意条件下都能自发进行 | |
| B. | 已知热化学方程式2A(g)+B(g)?2C (g)△H=-QkJ/mol (Q>0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出QkJ的热量 | |
| C. | 1mol/L的盐酸与1mol/L的氨水、11mol/L的NaOH溶液等体积混合,充分反应,后者比前者放出的热量多 | |
| D. | BaCl2溶液中加过量H2SO4,溶液中一定不存在Ba2+ |
10.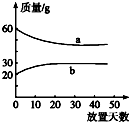 浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )
浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )
 浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )
浓硫酸和2mol•L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )| A. | a升华、b冷凝 | B. | a冷凝、b吸水 | C. | a挥发、b潮解 | D. | a挥发、b吸水 |
8.下列有关热化学方程式的书写及对应的表述均正确的是( )
0 153951 153959 153965 153969 153975 153977 153981 153987 153989 153995 154001 154005 154007 154011 154017 154019 154025 154029 154031 154035 154037 154041 154043 154045 154046 154047 154049 154050 154051 154053 154055 154059 154061 154065 154067 154071 154077 154079 154085 154089 154091 154095 154101 154107 154109 154115 154119 154121 154127 154131 154137 154145 203614
| A. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ•mol-1 | |
| B. | 稀盐酸与0.1 mol•L-1 KOH溶液反应:H+(aq)+OH-(aq)═H2O(l)△H=+57.3 kJ•mol-1 | |
| C. | 已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| D. | 已知2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则可知C的燃烧热△H=-110.5 kJ•mol-1 |