题目内容
16.下列说法正确的是( )| A. | 物质发生化学反应时必然伴随着能量变化 | |
| B. | 金属铜导电,故金属铜是电解质 | |
| C. | 自发反应都是熵增大的反应 | |
| D. | 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大 |
分析 A、化学反应的过程是旧键断裂新键形成的过程,断键成键都有能量变化;
B、铜是单质,而电解质是化合物;
C、根据△G=△H-T•△S判断;
D、增大反应物浓度,可增大单位体积内活化分子数,但百分数不变.
解答 解:A、化学反应的过程是旧键断裂新键形成的过程,断键成键都有能量变化,故A正确;
B、铜是单质,而电解质是化合物,铜是单质,不是电解质,也不是非电解质,故B错误;
C、根据△G=△H-T•△S可知,自发反应不一定都是熵增大的反应,也可能是低温熵减的反应,故C错误;
D、增大反应物浓度,可增大单位体积内活化分子数,从而使反应速率增大,而不是增大单位体积内活化分子的百分数,单位体积内活化分子的百分数是不变的,故D错误;
故选A.
点评 本题考查学生反应的热效应、电解质、反应的自发性和化学反应速率的知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
7.NA 为阿伏加德罗常数,下列叙述正确的是( )
| A. | 22.4LCl2完全溶于水时转移的电子数为NA | |
| B. | 1 mol 甲基(-CH3)含有的电子数为9NA | |
| C. | 100g30%醋酸溶液中氢原子数为2NA | |
| D. | 100mL水中OH-的个数是10-8NA |
4.下表符号中“2”的含义正确的一组是( )
| 2H | 2He | 2Cl | Ca2+ | |
| A | 质量数 | 中子数 | 质子数 | 电荷数 |
| B | 质量数 | 质子数 | 原子个数 | 电荷数 |
| C | 质子数 | 中子数 | 原子个数 | 电荷数 |
| D | 质量数 | 质子数 | 中子数 | 电荷数 |
| A. | A | B. | B | C. | C | D. | D |
11.下列说法正确的是( )
| A. | 放热反应在任意条件下都能自发进行 | |
| B. | 已知热化学方程式2A(g)+B(g)?2C (g)△H=-QkJ/mol (Q>0)将2molA(g)和1molB(g)置于一密闭容器中充分反应后放出QkJ的热量 | |
| C. | 1mol/L的盐酸与1mol/L的氨水、11mol/L的NaOH溶液等体积混合,充分反应,后者比前者放出的热量多 | |
| D. | BaCl2溶液中加过量H2SO4,溶液中一定不存在Ba2+ |
1.将5.6g铁粉放入一定量某浓度的硝酸溶液中,待铁粉全部溶解后,共收集到NO、NO2(其他气体忽略不计)混合气体0.15mol,该混合气体中NO与NO2的体积比可能是( )
| A. | 1:1 | B. | 2:1 | C. | 3:2 | D. | 3:1 |
8.下列实验操作能够达到实验目的是( )
| A. | 从溴水中提纯单质溴的方法是:先用CCl4萃取,分液后再蒸馏 | |
| B. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| C. | 用盛NaOH溶液的洗气瓶除去CO2中混有的HCl气体 | |
| D. | 在实验室里,用澄清的石灰水和氯化铵溶液混合制取氨气 |
5.下列叙述或离子方程式书写正确的是( )
| A. | 将少量二氧化硫通入次氯酸钠溶液中:SO2+H2O+3ClO-═SO42-+Cl-+2HClO | |
| B. | 向含有Fe2O3悬浊液中通入HI气体:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应:Ba2++2OH-+2NH4++SO42-═BaSO4↓+2NH3•H2O |
6.亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,主要用于棉纺、纸浆等漂白.NaClO2溶液中可生成ClO2、HClO2、ClO2-、Cl-等四种含氧微粒,经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出).则下列分析不正确的是( )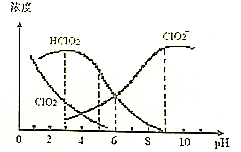

| A. | 向亚氯酸钠溶液加水稀释,溶液中n(ClO2)增大 | |
| B. | HClO2的电离平衡常数Ka=1.0×10-6 | |
| C. | NaClO2溶液中:c(Na+)+c(H+)>c(ClO2-)+c(Cl-) | |
| D. | pH=5时含氯元素的微粒浓度大小关系为:c(HClO2)>c(ClO2-)>c(Cl-)>c(ClO2) |