1. (1)某温度时,在3L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如下图所示.由图中数据分析:
(1)某温度时,在3L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如下图所示.由图中数据分析:
①该反应的化学方程式:Y+2Z?3X
②反应开始至2min末,X的反应速率为$\frac{1}{15}$mol/(L•min).
③该反应是由正逆反应同时开始反应的.(填“正反应”、“逆反应”或“正、逆反应同时”)
(2)在100℃时,将0.100mol N2O4气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到如表数据:
①该反应的平衡常数表达式为$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$;从表中分析:c1<c2,
c3=c4(填“>”、“<”或“=”).
②在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为0.001mol•L-1•s-1.
③达平衡后下列条件的改变可使NO2气体浓度增大的是B(填字母序号).
A.扩大容器的容积 B.再充入一定量的N2O4
C.分离出一定量的NO2 D.再充入一定量的He
④若在相同条件下,起始时只充入0.080mol NO2气体,则达到平衡时NO2气体的转化率为25%.
 (1)某温度时,在3L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如下图所示.由图中数据分析:
(1)某温度时,在3L密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如下图所示.由图中数据分析:①该反应的化学方程式:Y+2Z?3X
②反应开始至2min末,X的反应速率为$\frac{1}{15}$mol/(L•min).
③该反应是由正逆反应同时开始反应的.(填“正反应”、“逆反应”或“正、逆反应同时”)
(2)在100℃时,将0.100mol N2O4气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol•L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol•L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
c3=c4(填“>”、“<”或“=”).
②在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为0.001mol•L-1•s-1.
③达平衡后下列条件的改变可使NO2气体浓度增大的是B(填字母序号).
A.扩大容器的容积 B.再充入一定量的N2O4
C.分离出一定量的NO2 D.再充入一定量的He
④若在相同条件下,起始时只充入0.080mol NO2气体,则达到平衡时NO2气体的转化率为25%.
20.按图甲进行实验,若乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是( )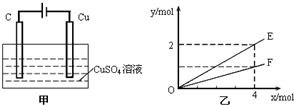

| A. | E表示生成铜的物质的量 | B. | E表示生成硫酸的物质的量 | ||
| C. | F表示反应消耗水的物质的量 | D. | E表示反应生成氧气的物质的量 |
19.下列溶液中,有关物质的量浓度关系正确的是( )
| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)═c(NO3-) | |
| B. | 0.1mol/L某二元弱酸强碱盐NaHA溶液中:c(Na+)═2c(A2-)+c(HA-)+c(H2A) | |
| C. | 10mL0.5mol/L CH3COONa溶液与6mL1mol/L盐酸混合c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| D. | 常温下,0.1mol/L pH=4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
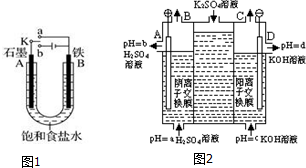
17.如图所示,甲池的总反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O.下列说法正确的是( )
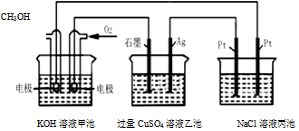

| A. | 甲池是电能转化为化学能的装置,乙、丙池是化学能转化电能的装置 | |
| B. | 甲池通入CH3OH的电极反应为CH3OH-6e-+2H2O═CO32-+8H+ | |
| C. | 甲池中消耗280mL(标准状况下)O2,此时乙池中银极增重1.6g | |
| D. | 反应一段时间后,向丙池中加入一定量盐酸,一定能使NaCl溶液恢复到原浓度 |
16.以下说法不正确的是( )
| A. | 1mol乙醇可以与足量金属钠反应,生成0.5molH2,能证明乙醇分子有一个H原子与其余的H原子不同 | |
| B. | 下列反应可证明苯环受甲基的影响,甲苯易被酸性高锰酸钾氧化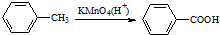 | |
| C. | 下列反应可证明由于羟基对苯环的影响,导致苯酚的取代比苯容易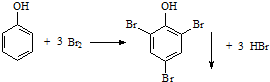 | |
| D. | 苯不能使溴的四氯化碳溶液褪色可以说明苯分子中没有与乙烯分子中类似的碳碳双键 |
15.下列有关热化学方程式的叙述正确的是( )
0 153474 153482 153488 153492 153498 153500 153504 153510 153512 153518 153524 153528 153530 153534 153540 153542 153548 153552 153554 153558 153560 153564 153566 153568 153569 153570 153572 153573 153574 153576 153578 153582 153584 153588 153590 153594 153600 153602 153608 153612 153614 153618 153624 153630 153632 153638 153642 153644 153650 153654 153660 153668 203614
| A. | 已知甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═2CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知中和热为△H=-57.3 kJ/mol,则1mol稀硫酸和足量稀NaOH溶液反应的反应热就是中和热 | |
| D. | 已知S(g)+O2(g)═SO2(g)△H1;S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 |
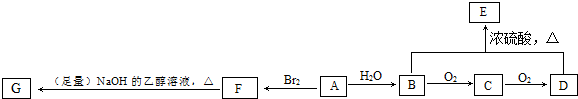
 )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下: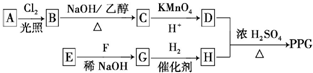
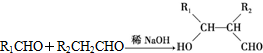

 .
. .
. .
.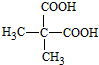
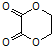 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.