题目内容
4.某烃A,可做水果的催熟剂,其蒸汽密度是氢气密度的14倍.一定条件下,它能发生如下的转化(已知:2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH,框图中部分生成物略去).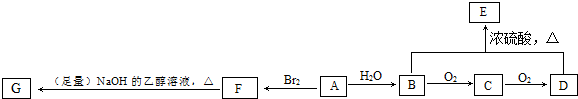
(1)写出A→B的反应方程式:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH
(2)写出B+D→E的反应方程式:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,反应类型为酯化反应或取代反应
(3)写出F→G的反应方程式:BrCH2CH2Br+2NaOH$→_{△}^{醇}$HC≡CH↑+2NaBr+2H2O,反应类型为消去反应.
分析 某烃A,其蒸汽密度是氢气密度的14倍,其相对分子质量为14×2=28,可做水果的催熟剂,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生氧化反应生成C为CH3CHO,乙醛进一步发生氧化反应生成D为CH3COOH,乙酸与乙醇发生酯化反应得到E为CH3COOCH2CH3.乙烯与溴发生加成反应得到F为BrCH2CH2Br,F发生消去反应生成G为HC≡CH.
解答 解:某烃A,其蒸汽密度是氢气密度的14倍,其相对分子质量为14×2=28,可做水果的催熟剂,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生氧化反应生成C为CH3CHO,乙醛进一步发生氧化反应生成D为CH3COOH,乙酸与乙醇发生酯化反应得到E为CH3COOCH2CH3.乙烯与溴发生加成反应得到F为BrCH2CH2Br,F发生消去反应生成G为HC≡CH.
(1)A→B的反应方程式:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,
故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;
(2)B+D→E的反应方程式:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,反应类型为 酯化反应或取代反应,
故答案为:CH3COOH+C2H5OH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;酯化反应或取代反应;
(3)F→G的反应方程式:BrCH2CH2Br+2NaOH$→_{△}^{醇}$HC≡CH↑+2NaBr+2H2O,反应类型为消去反应,
故答案为:BrCH2CH2Br+2NaOH$→_{△}^{醇}$HC≡CH↑+2NaBr+2H2O;消去反应.
点评 本题考查有机物推断,涉及烯烃、醇、醛、羧酸、卤代烃的性质与转化,关键是确定A为乙烯,再根据反应条件进行推断,侧重对基础知识的巩固.

| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)═c(NO3-) | |
| B. | 0.1mol/L某二元弱酸强碱盐NaHA溶液中:c(Na+)═2c(A2-)+c(HA-)+c(H2A) | |
| C. | 10mL0.5mol/L CH3COONa溶液与6mL1mol/L盐酸混合c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| D. | 常温下,0.1mol/L pH=4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
| A. | 氢氧化钠溶液中通入氯气:Cl2+OH-═ClO-+Cl-+H2O | |
| B. | 铁与硫酸铁溶液反应:Fe+Fe3+═2Fe2+ | |
| C. | 氢氧化镁与稀盐酸反应:Mg(OH)2+2H+═Mg2++2H2O | |
| D. | 碳酸氢钠溶液中滴入氢氧化钠溶液:OH-+HCO${\;}_{3}^{-}$═H2O+CO2↑ |
| A. |  太阳能生热器 | B. |  硅太阳能电池 | C. |  燃气灶 | D. |  锂离子电池 |
 .请写出1-丙醇与乙酸反应的化学方程式为CH3CH2CH2OH+CH3COOH
.请写出1-丙醇与乙酸反应的化学方程式为CH3CH2CH2OH+CH3COOH CH3COOCH2CH2CH3+H2O
CH3COOCH2CH2CH3+H2O