题目内容
3.某课外活动小组用如图1所示装置进行实验,请回答下列问题: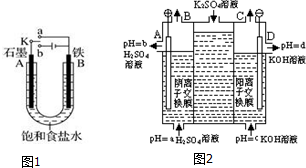
(1)若开始实验时开关K与a连接,则A极的电极反应式为O2+2H2O+4e-=4OH-
(2)若开始时开关K与b连接,下列说法正确的是①③(填序号).
①从A极处逸出的气体能使湿润淀粉KI试纸变蓝
②反应一段时间后,加适量盐酸可恢复到电解前电解质的浓度
③若标准状况下B极产生22.4L气体,则溶液中转移0.2mol电子
(3)根据氯碱工业原理用如图2所示装置电解K2SO4溶液.
①该电解槽的阳极反应式为4OH--4e-=2H2O+O2↑,通过阴离子交换膜的离子数<(填“>”、”=”或“<”)通过阳离子交换膜的离子数.
②图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为b<a<c<d.
③电解一段时间后,B口与C口产生气体的质量比为8:1.
分析 (1)若开始实验时开关K与a连接,铁为负极,发生铁的吸氧腐蚀;
(2)若开始时开关K与b连接时,两极均有气体产生,则Fe作阴极,石墨作阳极,阳极上氯离子放电、阴极上氢离子放电,据此回答.
(3)①电解硫酸钾溶液,阳极发生氧化反应,OH-被氧化生成O2;SO42-通过阴离子交换膜向阳极移动,钾离子通过阳离子交换膜向阴极移动;
②OH-被氧化,阳极生成H+和O2,pH减小,阴极发生还原反应生成H2和OH-,pH增大;
③B口生成氧气,C生成氢气.
解答 解:(1)开始时开关K与a连接,是原电池,铁为负极,发生氧化反应,失去电子生成亚铁离子,电极方程式为Fe-2e-=Fe2+,A极上氧气得电子被还原,电极方程式为O2+2H2O+4e-=4OH-,
故答案为:O2+2H2O+4e-=4OH-;
(2)K与b连接,为电解池,若开始时开关K与b连接时,两极均有气体产生,则Fe作阴极,石墨作阳极,氯离子、氢离子放电,电解的总离子反应为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,
①从A电极逸出的气体是氯气,能使湿润的KI淀粉试纸变蓝,故正确;
②电解的总离子反应为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,反应一段时间后通入HCl可恢复到电解前电解质的浓度,故错误;
③若标准状况下B电极产生2.24L即0.1mol氢气气体,则溶液中转移0.2mol电子,故正确.
故答案为:①③;
(3)①电解硫酸钾溶液,阳极发生氧化反应,OH-被氧化生成O2,电极方程式为,SO42-通过阴离子交换膜向阳极移动,钾离子通过阳离子交换膜向阴极移动,由电荷守恒知钾离子数目大于硫酸根离子数目,
故答案为:4OH--4e-=2H2O+O2↑;<;
②OH-被氧化,阳极生成H+和O2,pH减小,阴极发生还原反应生成H2和OH-,pH增大,则pHb<a<c<d,故答案为:b<a<c<d;
③B口生成氧气,C生成氢气,物质的量之比为1:2,则质量之比为32:4=8:1,故答案为:8:1.
点评 本题考查原电池和电解池知识,为高考常见题型和高频考点,侧重于学生的分析能力和电化学知识的综合运用,注意把握电极的判断和电极方程式的书写,为解答该题的关键,结合两极转移电离相等计算,难度中等.

| A. | 在溴乙烷中直接加入AgNO3溶液 | |
| B. | 加蒸馏水,充分搅拌后,加入AgNO3溶液 | |
| C. | 加入NaOH的乙醇溶液,加热后加入AgNO3溶液 | |
| D. | 加入NaOH溶液加热,冷却后加入稀硝酸酸化,然后加入AgNO3溶液 |
| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/(g/100g水) |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
(2)醇可发生分子内脱水生成烯烃,如C2H5OH$?_{170℃}^{浓硫酸}$CH2═CH2↑+H2O
请回答有关问题
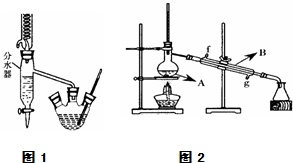
Ⅰ.乙酸正丁酯粗产品的制备
在三孔圆底烧瓶中装入沸石,加入18.5mL正丁醇和15.4mL冰醋酸(稍过量),再加3~4滴浓硫酸.然后安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管,加热冷凝回流反应.
(1)三孔烧瓶和蒸馏烧瓶在加热时都需要加入沸石,加入沸石是作用是防暴沸.本实验过程中可能产生多种有机副产品,请写成其中一种的结构简式CH3CH2CH2CH2OCH2CH2CH2CH3或CH2=CHCH2CH3.
(2)反应时加热有利于提高酯的产率,但实验发现温度过高酯的产率反而降低,可能的原因是乙酸、正丁醇都易挥发,温度过高可能使乙酸、正丁醇大量挥发使产率降低,温度过高可能发生副反应使产率降低.
Ⅱ.乙酸正丁酯粗产品的精制.
(3)将三孔圆底烧瓶中的产物转入分液漏斗中,并用饱和Na2CO3溶液洗涤有机层,接下来进行的操作名称是分液.
(4)将酯层采用如图2所示装置蒸馏.
①图2中仪器B的名称为冷凝管,水的流向应该从g(“f”或“g”)口进入.
②蒸馏收集乙酸正丁酯粗产品时,应将温度控制在126.1℃左右.
| A. | K+、Fe2+、Cl-、NO${\;}_{3}^{-}$ | B. | Na+、Ba2+、Cl-、SO${\;}_{4}^{2-}$ | ||
| C. | NH${\;}_{4}^{+}$、Fe3+、Cl-、SCN- | D. | K+、Mg2+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ |
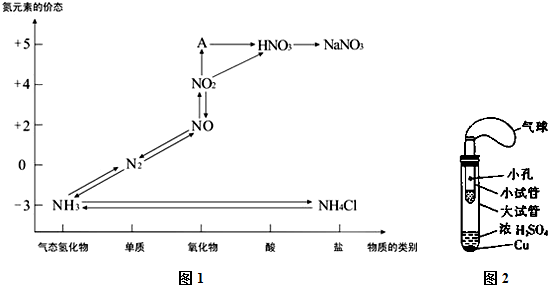
 )是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下:
)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景.PPG的一种合成路线如下: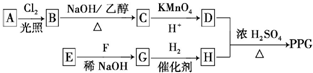

 .
. .
. .
.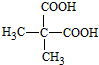
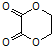 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2Br$→_{加热}^{NaOH/醇}$CH2=CH2$→_{催化剂}^{H_{2}O}$CH3CH2OH.