12.配合物Na2[Fe(CN)5(NO)]可用于离子检验,此配合物中不存在的化学键是( )
| A. | 离子键 | B. | 金属键 | C. | 氢键 | D. | 极性共价键 |
11.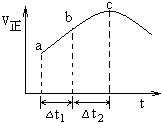 向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)═SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)═SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
 向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)═SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )
向绝热恒容密闭容器中通入SO2和NO2,在一定条件下使反应SO2(g)+NO2(g)═SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如图所示.由图可得出的正确结论是( )| A. | 该反应为放热反应 | |
| B. | 反应物浓度:c>b>a | |
| C. | a、b均未建立平衡,c点恰好达到平衡 | |
| D. | 若在恒温恒容容器中,以相同的投料进行该反应,平衡后转化率小于绝热恒容容器中的转化率 |
9.在0.1mol•L-1 Na2CO3溶液中,欲使CO32-的浓度尽量接近0.1mol•L-1,则应向溶液中加( )
| A. | HCl | B. | Na2CO3 | C. | NaCl | D. | KOH |
8. 车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
(1)写出NO与活性炭反应的化学方程式C+2NO?N2+CO2;
(2)计算上述反应T1℃时的平衡常数K1=4;
(3)上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为80%;
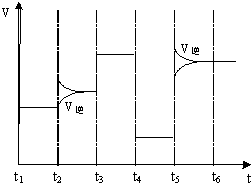
(4)如图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一个反应条件,平衡体系中反应速率随时间变化的情况,且所改变的条件均不同.已知t3-t4阶段为使用催化剂.请判断该反应△H<0(填“>”或“<”).
 车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:
车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”.活性炭可处理大气污染物NO.在5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量(n/mol)如表:| 物质 T/℃ | 活性炭 | NO | E | F |
| 初始 | 3.000 | 0.10 | 0 | 0 |
| T1 | 2.960 | 0.020 | 0.040 | 0.040 |
| T2 | 2.975 | 0.050 | 0.025 | 0.025 |
(2)计算上述反应T1℃时的平衡常数K1=4;
(3)上述反应T1℃时达到化学平衡后再通入0.1molNO气体,则达到新化学平衡时NO的转化率为80%;
(4)如图为在T1℃达到平衡后在t2、t3、t4、t5时改变某一个反应条件,平衡体系中反应速率随时间变化的情况,且所改变的条件均不同.已知t3-t4阶段为使用催化剂.请判断该反应△H<0(填“>”或“<”).
6.下列关于金属元素特征的叙述中,正确的是( )
①金属元素的原子只有还原性,离子只有氧化性
②金属元素在化合物中都显正价
③元素的金属性越强,相应的离子氧化性越弱
④失电子数越多,元素的金属性越强.
①金属元素的原子只有还原性,离子只有氧化性
②金属元素在化合物中都显正价
③元素的金属性越强,相应的离子氧化性越弱
④失电子数越多,元素的金属性越强.
| A. | .①②③ | B. | ②③ | C. | ① | D. | 全部 |
3.某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
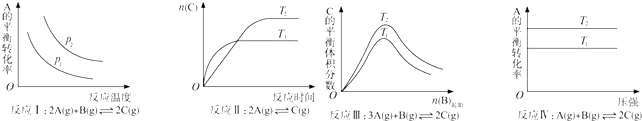
根据以上规律判断,上列结论正确的是( )
0 153146 153154 153160 153164 153170 153172 153176 153182 153184 153190 153196 153200 153202 153206 153212 153214 153220 153224 153226 153230 153232 153236 153238 153240 153241 153242 153244 153245 153246 153248 153250 153254 153256 153260 153262 153266 153272 153274 153280 153284 153286 153290 153296 153302 153304 153310 153314 153316 153322 153326 153332 153340 203614

根据以上规律判断,上列结论正确的是( )
| A. | 反应Ⅰ:△H>0,P2>P1 | B. | 反应Ⅱ:△H<0,T1>T2 | ||
| C. | 反应Ⅲ:△H>0,T2<T1;或△H<0,T2>T1 | D. | 反应Ⅳ:△H<0,T2>T1 |
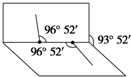 解答下列问题,本题共两个小题.
解答下列问题,本题共两个小题.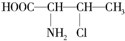 ,一个该有机物分子中含有2个手性碳原子.其中一对对映异构体用简单的投影式表示为:
,一个该有机物分子中含有2个手性碳原子.其中一对对映异构体用简单的投影式表示为: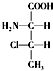 和
和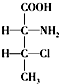 ,则另一对对映异构体的简单投影式为:
,则另一对对映异构体的简单投影式为: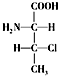 和
和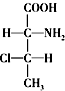 .②②
.②②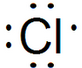 .
.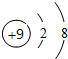 .
.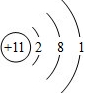 D2-的电子式为
D2-的电子式为 .
. ;Z元素原子的电子式为
;Z元素原子的电子式为 .
.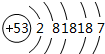 .
.