6.向Cu、Fe和Fe2O3的混合物中加入稀硫酸发生反应.下列说法正确的是( )
| A. | 反应后溶液可能呈中性 | |
| B. | 反应停止后一定有固体剩余 | |
| C. | 反应过程中一定有氧化还原反应发生 | |
| D. | 若只有Cu剩余,向溶液中滴入铁氰化钾溶液不会产生蓝色沉淀 |
5.25℃时,1mol/L醋酸加水稀释至0.01mol/L,关于稀释前后的下列变化正确的是( )
| A. | 溶液中c(OH-)减小 | B. | pH的变化值等于2 | ||
| C. | 溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$的值增大 | D. | Kw的值减小 |
4.下列解释实验事实的方程式正确的是( )
| A. | 用氢氧化钠溶液去除铝条表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| B. | 铜片溶于稀硝酸产生无色气体:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | 氢氧化亚铁在空气中变质:2Fe(OH)2+O2+2H2O═2Fe(OH)3 | |
| D. | 碳酸钠溶液呈碱性:CO32-+2H2O?H2CO3+2OH- |
3.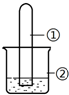 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
 用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )| 选项 | ①中的物质 | ②中的物质 | 预测装置中现象 |
| A | NO2 | 蒸馏水 | 试管充满无色溶液 |
| B | SO2 | 紫色石蕊溶液 | 溶液逐渐变为红色 |
| C | NH3 | AlCl3溶液 | 产生白色沉淀 |
| D | Cl2 | AgNO3溶液 | 产生白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
2.某化学小组欲探究FeCl3溶液、FeCl2溶液的化学性质
(1)试剂清单:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、碘化钾、淀粉溶液.
查阅资料得知:淀粉遇I2变蓝.
请帮助他们完成以下实验报告:
填空:
①验证Fe2+具有还原性③2Fe2++Cl2══2Fe3++2Cl- ⑤证明Fe2+具有氧化性⑧2Fe3++Fe══3Fe2+⑩证明Fe3+具有氧化性
综合以上实验,你能得到的结论是:⑪Fe3+有氧化性;Fe2+既有氧化性,又有还原性.
(2)除了以上性质,你认为FeCl2还可能具有的性质是:(用离子方程式表示,任写一个即可Fe2++2OH-=2Fe(OH)2↓.
(3)亚铁盐在溶液中易被氧化,而实验中需要纯净的亚铁盐溶液.保存亚铁盐溶液时如何防止亚铁盐被氧化加入少量铁粉.
(4)检验某溶液是Fe2+溶液的方法是(任写一种试剂及其对应的现象即可):加入KSCN溶液,无现象,再加入氯水(双氧水等合理氧化剂),溶液变血红色,或者加入K3[Fe(CN)6]产生蓝色沉淀.
(5)某同学向FeCl2中加入NaClO溶液,产生红褐色沉淀,你认为该反应中产生红褐色沉淀的原因可能是NaClO将Fe2+氧化为Fe3+,Fe3+转化为Fe(OH)3沉淀.
(1)试剂清单:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、碘化钾、淀粉溶液.
查阅资料得知:淀粉遇I2变蓝.
请帮助他们完成以下实验报告:
| 序号 | 实验 目的 | 实验内容 | 实验现象 | 实验结论 | 离子方程式 |
| 实验1 | ① | 在FeCl2溶液中滴入适量 氯水 | 溶液由浅绿色 变为黄色 | ② | ③ |
| 实验2 | ④ | 在FeCl2溶液中加入锌片 | / | ⑤ | Zn+Fe2+═Zn2++Fe |
| 实验3 | ⑥ | 在FeCl3溶液中加入足量 铁粉 | ⑦ | FeCl3(Fe3+)具有氧化性 | ⑧ |
| 实验4 | ⑨ | 在FeCl3溶液中滴入适量KI溶液和 淀粉溶液 | 淀粉溶液变蓝 | ⑩ | 2Fe3++2I-═2Fe2++I2 |
①验证Fe2+具有还原性③2Fe2++Cl2══2Fe3++2Cl- ⑤证明Fe2+具有氧化性⑧2Fe3++Fe══3Fe2+⑩证明Fe3+具有氧化性
综合以上实验,你能得到的结论是:⑪Fe3+有氧化性;Fe2+既有氧化性,又有还原性.
(2)除了以上性质,你认为FeCl2还可能具有的性质是:(用离子方程式表示,任写一个即可Fe2++2OH-=2Fe(OH)2↓.
(3)亚铁盐在溶液中易被氧化,而实验中需要纯净的亚铁盐溶液.保存亚铁盐溶液时如何防止亚铁盐被氧化加入少量铁粉.
(4)检验某溶液是Fe2+溶液的方法是(任写一种试剂及其对应的现象即可):加入KSCN溶液,无现象,再加入氯水(双氧水等合理氧化剂),溶液变血红色,或者加入K3[Fe(CN)6]产生蓝色沉淀.
(5)某同学向FeCl2中加入NaClO溶液,产生红褐色沉淀,你认为该反应中产生红褐色沉淀的原因可能是NaClO将Fe2+氧化为Fe3+,Fe3+转化为Fe(OH)3沉淀.
1.某小组同学采用以下装置验证SO2的性质:(夹持及加热装置略)
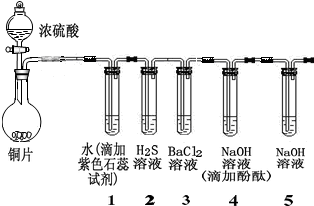
(1)写出圆底烧瓶中发生反应的化学方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)从实验目的分析,试管1、4的目的都是为了证明SO2具有酸性氧化物的通性(性质),试管2是为了证明SO2具有氧化性(性质).
(3)除上述两种性质外,你认为SO2还具有的性质是还原性(或漂白性),可以通过加入KMnO4溶液(或品红)(填试剂化学式或者名称)加以证明.
(4)经过实验,观察到如下实验现象:
①试管1中紫色石蕊溶液变红.
②试管2中有浅黄色浑浊出现,写出反应的化学方程式2H2S+SO2=3S↓+2H2O.
(5)试管4中无明显现象,将其分成两份,分别加入下列物质均产生沉淀.将产生的沉淀的化学式填入下表相应位置.
(6)试管4和试管5均加入NaOH溶液,在实验目的上的不同点是3是验证性质,5是吸收.

(1)写出圆底烧瓶中发生反应的化学方程式:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O.
(2)从实验目的分析,试管1、4的目的都是为了证明SO2具有酸性氧化物的通性(性质),试管2是为了证明SO2具有氧化性(性质).
(3)除上述两种性质外,你认为SO2还具有的性质是还原性(或漂白性),可以通过加入KMnO4溶液(或品红)(填试剂化学式或者名称)加以证明.
(4)经过实验,观察到如下实验现象:
①试管1中紫色石蕊溶液变红.
②试管2中有浅黄色浑浊出现,写出反应的化学方程式2H2S+SO2=3S↓+2H2O.
(5)试管4中无明显现象,将其分成两份,分别加入下列物质均产生沉淀.将产生的沉淀的化学式填入下表相应位置.
| 加入的物质 | O2 | 氨水 |
| 沉淀的化学式 |
18.除去下列物质中的杂质(括号内为杂质),所选用的试剂不正确的一组是( )
| 选项 | 待提纯的物质 | 选用试剂 |
| A | FeCl3溶液(FeCl2溶液) | Cl2 |
| B | NaCl溶液(Na2SO4溶液) | Ba(NO3)2溶液 |
| C | Cl2(HCl) | 饱和食盐水 |
| D | CO2(SO2) | 酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
17.下列实验方法或操作能达到实验目的是( )
0 152597 152605 152611 152615 152621 152623 152627 152633 152635 152641 152647 152651 152653 152657 152663 152665 152671 152675 152677 152681 152683 152687 152689 152691 152692 152693 152695 152696 152697 152699 152701 152705 152707 152711 152713 152717 152723 152725 152731 152735 152737 152741 152747 152753 152755 152761 152765 152767 152773 152777 152783 152791 203614
| A. | 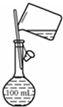 配制150mL 0.1 mol/L盐酸 | B. |  验证氨水呈碱性 | ||
| C. | 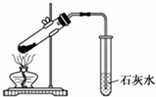 探究NaHCO3的热稳定性 | D. | 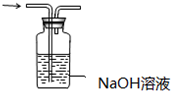 除去二氧化碳中的氯化氢 |