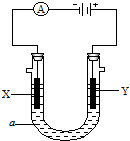
18.化学知识在生产和生活中有着重要的应用.下列说法中不正确的是( )
①钠的还原性很强,可以置换出硫酸铜溶液中的铜单质
②氧化铝可制作耐火坩埚,只因为氧化铝的化学性质很稳定
③发酵粉中含有碳酸氢钠,能使焙制出的糕点疏松多孔
④Na2O2和Na2O均可作呼吸面具中O2的来源
⑤明矾常作为消毒剂
⑥碳酸钠在医疗上是治疗胃酸过多的一种药剂.
①钠的还原性很强,可以置换出硫酸铜溶液中的铜单质
②氧化铝可制作耐火坩埚,只因为氧化铝的化学性质很稳定
③发酵粉中含有碳酸氢钠,能使焙制出的糕点疏松多孔
④Na2O2和Na2O均可作呼吸面具中O2的来源
⑤明矾常作为消毒剂
⑥碳酸钠在医疗上是治疗胃酸过多的一种药剂.
| A. | ①②③④ | B. | ①②④⑤ | C. | ①②③④⑥ | D. | ①②④⑤⑥ |
16.在0.5L的密闭容器中,一定量的H2和N2进行如下化学反应:3H2(g)+N2(g)═2NH3(g)△H<0,其化学平衡常数K与温度t的关系如下表.请回答下列问题.
①比较K1,K2的大小,K1>K2(填写“>”、“=”或“<”).
②在400℃时,当测得NH3和N2、H2的物质的量分别为3mol和1mol、2mol时,则该反应的 V(H2)正> V (H2)逆(填写“>”、“=”或“<”).
| t/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
②在400℃时,当测得NH3和N2、H2的物质的量分别为3mol和1mol、2mol时,则该反应的 V(H2)正> V (H2)逆(填写“>”、“=”或“<”).
15.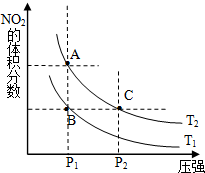 (1)对反应N2O4(g)═2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.T1<T2(填“>”、“<”或“=”);A、C两点的速率VA<VC(同上).
(1)对反应N2O4(g)═2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.T1<T2(填“>”、“<”或“=”);A、C两点的速率VA<VC(同上).
(2)在100℃时,将0.400mol的NO2气体充入2L真空定容密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
①该反应的平衡常数K的值为2.78;
②若在相同情况下最初向该容器充入的是N2O4,要达到上述同样的平衡状态,N2O4的起始浓度是0.1mol/L.
③计算②中条件下达到平衡后混合气体的平均相对分子质量为57.5;(结果保留小数点后一位)
 (1)对反应N2O4(g)═2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.T1<T2(填“>”、“<”或“=”);A、C两点的速率VA<VC(同上).
(1)对反应N2O4(g)═2NO2(g)△H>0,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.T1<T2(填“>”、“<”或“=”);A、C两点的速率VA<VC(同上).(2)在100℃时,将0.400mol的NO2气体充入2L真空定容密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
②若在相同情况下最初向该容器充入的是N2O4,要达到上述同样的平衡状态,N2O4的起始浓度是0.1mol/L.
③计算②中条件下达到平衡后混合气体的平均相对分子质量为57.5;(结果保留小数点后一位)
14.设NA表示阿伏加德罗常数的数值,下列有关说法正确的是( )
| A. | 标准状况下,22.4 L 氯水中含有的分子数为NA | |
| B. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| C. | 1L 1mol•L-1的Na2CO3溶液中CO32-的数目为NA | |
| D. | 2.3 g金属钠与足量的氧气反应,无论加热与否转移电子数均为0.1NA |
12.( I )向一体积不变的密闭容器中充入2mol A,0.6mol C和一定量的B三种气体,一定条件下发生反应2A(g)+B(g)═3C(g),各物质的浓度随时间变化的关系如图 1所示,其中t0~t1阶段c(B)未画出.图2为反应体系中反应速率随时间变化的情况且t2,t3,t4各改变一种不同的条件.

(1)若t1=15min,则t0~t1阶段以C的浓度变化表示的反应速率v(C)=0.02mol/(L•min).
(2)t3时改变的条件为减小压强或取出部分平衡混合气体,B的起始物质的量为1mol,
(3)t4~t5阶段,若A的物质的量减少了0.01mol,而此阶段中反应体系吸收能量为a kJ,写出此条件下该反应的热化学方程式:2A(g)+B(g)?3C(g)△H=+200aKJ/mol.
(II)在容积可变的密闭容器中发生反应:mA(g)+nB(g)?pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表
(1)当压强从2×105 Pa增加到5×105 Pa时,平衡不移动(填:向左,向右,不)
(2)维持压强为2×105 Pa,当反应达到平衡状态时,体系中共有amol气体,再向体系中加入bmolB,当重新达到平衡时,体系中气体总物质的量是a+bmol.
(3)当压强为1×106 Pa时,此反应的平衡常数表达式:$\frac{[C]{\;}^{p}}{[A]^{m}}$.

(1)若t1=15min,则t0~t1阶段以C的浓度变化表示的反应速率v(C)=0.02mol/(L•min).
(2)t3时改变的条件为减小压强或取出部分平衡混合气体,B的起始物质的量为1mol,
(3)t4~t5阶段,若A的物质的量减少了0.01mol,而此阶段中反应体系吸收能量为a kJ,写出此条件下该反应的热化学方程式:2A(g)+B(g)?3C(g)△H=+200aKJ/mol.
(II)在容积可变的密闭容器中发生反应:mA(g)+nB(g)?pC(g),在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
(2)维持压强为2×105 Pa,当反应达到平衡状态时,体系中共有amol气体,再向体系中加入bmolB,当重新达到平衡时,体系中气体总物质的量是a+bmol.
(3)当压强为1×106 Pa时,此反应的平衡常数表达式:$\frac{[C]{\;}^{p}}{[A]^{m}}$.
10.在200mLMgCl2,AlCl3的混合溶液中,浓度为:MgCl2 2mol/L,AlCl3 3mol/L.现欲使其中的Mg2+转化为Mg(OH)2沉淀而从溶液中分离出来,至少需要0.8mol/LNaOH溶液的体积是( )
0 152469 152477 152483 152487 152493 152495 152499 152505 152507 152513 152519 152523 152525 152529 152535 152537 152543 152547 152549 152553 152555 152559 152561 152563 152564 152565 152567 152568 152569 152571 152573 152577 152579 152583 152585 152589 152595 152597 152603 152607 152609 152613 152619 152625 152627 152633 152637 152639 152645 152649 152655 152663 203614
| A. | 0.533L | B. | 0.267L | C. | 4.0L | D. | 2.0L |