 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),p(CO32-)=-lgc(CO32-).下列说法正确的是( )
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),p(CO32-)=-lgc(CO32-).下列说法正确的是( )| A、MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B、a点可表示MnCO3的饱和溶液,且c(Mn2+)<c(CO32-) |
| C、b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D、c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-) |
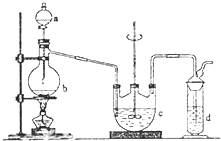
 如图装置,试管中盛有水,气球a中盛有干燥的Na2O2颗粒,U形管中注有浅红色的水,将气球用橡皮筋紧缚在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )
如图装置,试管中盛有水,气球a中盛有干燥的Na2O2颗粒,U形管中注有浅红色的水,将气球用橡皮筋紧缚在试管口.实验时将气球中的Na2O2抖落到试管b的水中,将发生的现象是( )| A、U形管内红色退去 |
| B、试管内溶液变红 |
| C、气球a变瘪 |
| D、U形管水位d>c |
工业生产硫酸可表示为:FeS2→SO2→SO3→H2SO4
已知:FeS2(s)+
O2(g)═
Fe2O3(s)+2SO2(g);△H═-853kJ?mol-1
2SO2(g)+O2(g)═2SO3(g);△H═-196.6kJ?mol-1
SO3(g)+H2O(l)═H2SO4(l);△H═-130.3kJ?mol-1
则1mol FeS2完全转化为H2SO4的反应热等于( )
已知:FeS2(s)+
| 11 |
| 4 |
| 1 |
| 2 |
2SO2(g)+O2(g)═2SO3(g);△H═-196.6kJ?mol-1
SO3(g)+H2O(l)═H2SO4(l);△H═-130.3kJ?mol-1
则1mol FeS2完全转化为H2SO4的反应热等于( )
| A、-130.3kJ?mol-1 |
| B、-1310.2kJ?mol-1 |
| C、-1179.kJ?mol-1 |
| D、-853kJ?mol-1 |
 在实验室中可通过如下反应制取硫代硫酸钠Na2S2O3:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2
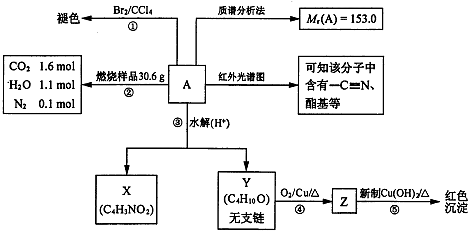
在实验室中可通过如下反应制取硫代硫酸钠Na2S2O3:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2 )是合成某种手术用粘合剂的单体,X的合成路线如下:
)是合成某种手术用粘合剂的单体,X的合成路线如下:

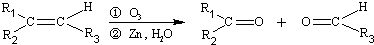 (R1、R2、R3代表烃基)
(R1、R2、R3代表烃基)
 :
:
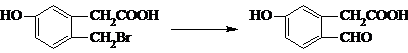
 属芳香醚,其同系物的通式为:
属芳香醚,其同系物的通式为:

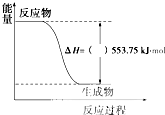 (1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:
(1)许多运动会使用的火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题: