题目内容
 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),p(CO32-)=-lgc(CO32-).下列说法正确的是( )
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lgc(M),p(CO32-)=-lgc(CO32-).下列说法正确的是( )| A、MgCO3、CaCO3、MnCO3的Ksp依次增大 |
| B、a点可表示MnCO3的饱和溶液,且c(Mn2+)<c(CO32-) |
| C、b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32-) |
| D、c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO32-) |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.pM相等时,图线中p(CO32-)数值越大,实际浓度越小;
B.a点可表示MnCO3的饱和溶液,pM=p(CO32-);
C.b点可表示CaCO3的饱和溶液,pM>p(CO32-);
D.pM数值越大,实际浓度越小,则c点可表示MgCO3 的不饱和溶液,pM>p(CO32-).
B.a点可表示MnCO3的饱和溶液,pM=p(CO32-);
C.b点可表示CaCO3的饱和溶液,pM>p(CO32-);
D.pM数值越大,实际浓度越小,则c点可表示MgCO3 的不饱和溶液,pM>p(CO32-).
解答:
解:A.pM相等时,图线中p(CO32-)数值越大,实际浓度越小,因此,MgCO3、CaCO3、MnCO3 的Ksp依次减小,故A错误;
B.a点可表示MnCO3的饱和溶液,pM=p(CO32-),所以c(Mn2+)=c(CO32-),故B错误;
C.b点可表示CaCO3的饱和溶液,pM>p(CO32-),所以c(Ca2+)<c(CO32-),故C正确;
D.pM数值越小,实际浓度越大,已知c点不在曲线上,而在曲线下面,则c点表示MgCO3 的过饱和溶液,pM>p(CO32-),所以c(Mg2+)<c(CO32-),故D错误;
故选:C.
B.a点可表示MnCO3的饱和溶液,pM=p(CO32-),所以c(Mn2+)=c(CO32-),故B错误;
C.b点可表示CaCO3的饱和溶液,pM>p(CO32-),所以c(Ca2+)<c(CO32-),故C正确;
D.pM数值越小,实际浓度越大,已知c点不在曲线上,而在曲线下面,则c点表示MgCO3 的过饱和溶液,pM>p(CO32-),所以c(Mg2+)<c(CO32-),故D错误;
故选:C.
点评:本题主要考查了沉淀溶解平衡曲线,掌握图线中pc(CO32-)、pM数值越大,实际浓度越小是解题的关键,难度中等.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
下列离子方程式涉及的反应属于氧化还原反应的是( )
| A、Ba2++SO42-═BaSO4↓ |
| B、Fe+2H+═Fe2++H2↑ |
| C、Al2O3+6H+═2Al3++3H2O |
| D、HCO3-+OH-═CO32-+H2O |
已知25℃时,AgCl的溶度积Ksp=1.8×10-10,则下列说法正确的是( )
| A、温度一定时,当溶液中c(Ag+)×c(Cl-)=Ksp时,此溶液为AgCl的饱和溶液 |
| B、AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) |
| C、向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| D、将固体AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,AgCl溶解度小于AgI |
工业生产硫酸可表示为:FeS2→SO2→SO3→H2SO4
已知:FeS2(s)+
O2(g)═
Fe2O3(s)+2SO2(g);△H═-853kJ?mol-1
2SO2(g)+O2(g)═2SO3(g);△H═-196.6kJ?mol-1
SO3(g)+H2O(l)═H2SO4(l);△H═-130.3kJ?mol-1
则1mol FeS2完全转化为H2SO4的反应热等于( )
已知:FeS2(s)+
| 11 |
| 4 |
| 1 |
| 2 |
2SO2(g)+O2(g)═2SO3(g);△H═-196.6kJ?mol-1
SO3(g)+H2O(l)═H2SO4(l);△H═-130.3kJ?mol-1
则1mol FeS2完全转化为H2SO4的反应热等于( )
| A、-130.3kJ?mol-1 |
| B、-1310.2kJ?mol-1 |
| C、-1179.kJ?mol-1 |
| D、-853kJ?mol-1 |
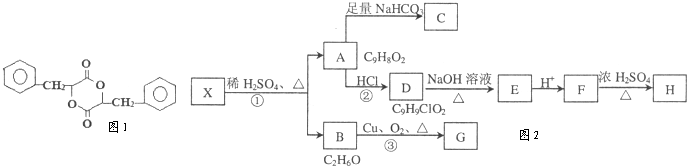

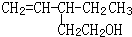 具有一定的光学活性,请你列举两种使该物质失去光学活性的方法
具有一定的光学活性,请你列举两种使该物质失去光学活性的方法