题目内容
19.“探险队员”盐酸,不小心走进了化学迷宫,迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过.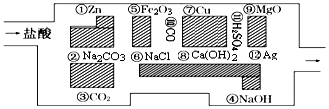
(1)请你帮助它走出迷宫(用图中物质前的序号连接起来表示所走的路线)③→⑥→⑩→⑦→⑪→⑫.
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有2个,属于氧化还原反应的有1个,写出反应的化学方程式并标明电子转移的方向和数目
 .其中氧化剂是HCl,还原剂是Zn.
.其中氧化剂是HCl,还原剂是Zn.(3)如果将盐酸换成氯化钡,它能沿着盐酸走出的路线“走出”这个迷宫吗?
填“能”或“不能”不能,若不能请写出离子方程式说明其原因:Ba2++SO42-=BaSO4↓.
分析 (1)解决该题应该找出一条不能和盐酸发生反应的物质构成的路.酸的化学性质有:能够和酸碱指示剂变色,能够和活泼金属反应,能够和金属氧化物反应,能够和碱反应,能够和某些盐反应,活泼金属即在金属活动性顺序表中氢前的金属,酸和金属氧化物、碱、盐发生的反应是复分解反应,因此必须有水、沉淀或气体生成;
(2)中和反应是酸与碱反应,根据碱的种类确定中和反应的个数;能与盐酸反应的盐只有碳酸钠;根据化合价变化判断氧化还原反应;
(3)如果将盐酸换成氯化钡,应该找出一条不能和氯化钡发生反应的物质构成的路.
解答 解:(1)利用图示的物质对相关的与盐酸不能反应的物质作出判断即可,由于盐酸不能和Cu、CO、硫酸、NaCl、Ag反应,
故答案为:③→⑥→⑩→⑦→⑪→⑫;
(2)中和反应是酸与碱反应,根据碱的种类确定中和反应的个数,碱有2种,则中和反应有2个; 盐酸和金属锌的反应中Zn元素化合价由0价变为+2价、H元素化合价由+1价变为0价,所以属于氧化还原反应,转移电子数为2,Zn是还原剂,盐酸是氧化剂,即转移电子方向和数目为 ,
,
故答案为:2;1; ;HCl;Zn;
;HCl;Zn;
(3)如果将盐酸换成氯化钡,它能沿着盐酸走出的路线“走出”这个迷宫,需要氯化钡和盐酸一样,和路线中的物质不能反应,但是氯化钡和硫酸之间反应,所以
将盐酸换成氯化钡,不能沿着盐酸走出的路线“走出”这个迷宫,离子方程式为Ba2++SO42-=BaSO4↓,故答案为:不能;Ba2++SO42-=BaSO4↓.
点评 本题考查物质的性质,为高频考点,综合考查元素化合物知识,把握金属及化合物的性质、反应类型及发生的反应为解答的关键,侧重分析能力及知识的应用能力和解决问题的能力的考查,题目难度不大.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
9.室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol/L的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )

| A. | 三种酸的电离常数关系:KHA>KHB>KHD | |
| B. | 滴定至P点时,溶液中:c(Na+)>c(B-)>c(HB)>c(H+)>c(OH-) | |
| C. | pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-) |
10.如图所示的实验,能达到实验目的或说法正确的是( )
| A. | 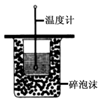 进行中和热的测定 | |
| B. | 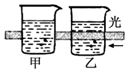 运用该实验可区分胶体和溶液 | |
| C. | 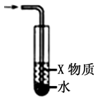 X若为苯,可用于吸收NH3或HCl,并防止倒吸 | |
| D. |  验证AgCl溶解度大于Ag2S |
4.下列有关化学用语表示正确的是( )
| A. | NH4Cl的电子式: | |
| B. | 对硝基甲苯: | |
| C. | 碳酸的电离方程式:H2CO3?2H++CO${\;}_{3}^{2-}$ | |
| D. | 硫离子的结构示意图: |
11.将石墨置于熔融的钾中,石墨会吸收钾而形成称为钾石墨的物质,其组成是C8K、C24K、C36K、C48K和C60K.在钾石墨中,钾元素处于石墨中间层,因而石墨层之间被胀大,层间距离增大,钾原子把最外层电子交给石墨层但在遇到与金属钾易反应的其它物质时还会收回.下列对钾石墨的叙述正确的是( )
| A. | 钾石墨是一类共价化合物 | B. | 钾石墨导电性比石墨强 | ||
| C. | 钾石墨遇水不产生氢气 | D. | C8K、C24K和C36K属于同素异形体 |
8.下列叙述中不正确的是( )
| A. | 常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为l×10-24,该溶液中一定可以大量存在K+、Na+、AlO-2、SO2-4 | |
| B. | 1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA | |
| C. | 镍镉可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd(OH)2+2Ni(OH)2$?_{放电}^{充电}$Cd(OH)2+2Ni(OH)2+2H2O,充电时阳极反应为:Ni(OH)2+OH-+e-═NiO(OH)+H2O | |
| D. | 某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O.已知As是产物之一,则该反应配平后H2O的化学计量数为6 |
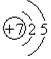
 欲配制 250mL0.1mol/L的NaOH溶液,回答下列有关问题:
欲配制 250mL0.1mol/L的NaOH溶液,回答下列有关问题: