题目内容
9.室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol/L的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )
| A. | 三种酸的电离常数关系:KHA>KHB>KHD | |
| B. | 滴定至P点时,溶液中:c(Na+)>c(B-)>c(HB)>c(H+)>c(OH-) | |
| C. | pH=7时,三种溶液中:c(A-)=c(B-)=c(D-) | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-) |
分析 A.根据等浓度的三种一元酸的PH大小确定三种酸的电离常数;
B.HB被中和一半时,溶液中溶质有中和生成的盐与未反应完的酸,根据盐的水解与酸的电离程度进行比较;
C.当PH=7时,三种溶液所消耗的氢氧化钠的体积不相同;
D.恰好中和时,三种溶液所消耗的氢氧化钠体积相同,生成三种盐的浓度相同,混合后根据盐的水解写出质子守恒解答.
解答 解:A.相同物质的量浓度的一元酸,酸的pH越小,氢离子浓度越大,说明酸的电离程度越大,则该酸的酸性越强,其电离平衡常数越大,根据图知,未加NaOH溶液时,pH:HA<HB<HD,说明酸的电离程度HA>HB>HD,则KHA>KHB>KHD,故A正确;
B.中和50%即P点,溶液中溶质为等物质的量浓度的酸(HB)和盐(NaB),由图可知溶液呈酸性,则c(H+)>c(OH-),且酸的电离程度大于酸根离子水解程度,
①NaB完全电离:NaB=Na++B-,这一步的c(B-)=c(Na+),
②HB少部分电离:HB?H++B-,则c(HB)>c(H+),
③NaB少部分水解:B-+H2O?HB+OH-,
由于酸的电离程度大于盐的水解程度,则HB电离产生的B-相对NaB水解消耗的B-多,所以c(B-)>c(Na+),由于HB电离消耗得多,水解生成的HB少,
所以c(Na+)>c(HB),则c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-),故B错误;
C.当pH=7时,根据电荷守恒三种溶液中离子浓度关系为:
c(Na+)+c(H+)=c(A-)+c(OH-),由于c(H+)=c(OH-),所以c(Na+)=c(A-),
c(Na+)+c(H+)=c(B-)+c(OH-),由于c(H+)=c(OH-),所以c(Na+)=c(B-),
c(Na+)+c(H+)=c(D-)+c(OH-),由于c(H+)=c(OH-),所以c(Na+)=c(D-),
由于三种酸根的水解程度不同,则溶液呈中性时所消耗的氢氧化钠的体积不相同,则三种溶液中钠离子浓度不同,c(A-)、c(B-)、c(D-)也不同,故C错误;
D.恰好中和时,三种溶液所消耗的氢氧化钠体积相同,生成三种盐的浓度相同,混合后溶液因盐的水解呈碱性,质子守恒的关系为:c(OH-)=c(HA)+c(HB)+c(HD)+c(H+),故D错误;
故选:A.
点评 本题以弱电解质的电离为载体考查酸碱混合溶液定性判断,明确电解质溶液中三大守恒以及酸的电离程度与酸根离子水解程度的大小是解题关键,题目难度中等.

| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)最高价氧化物的水化物碱性最强的是NaOH,酸性最强的是HClO4;
(3)A分别与D、E、F、G、H形成的化合物中,最稳定气态氢化物是HF;
(4)在B、C、F、H中,离子半径从大到小的顺序是S2->Cl->Na+>Al3+;
(5)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式OH-+Al(OH)3=AlO2-+2H2O.
C2H2(g)+H2(g)?C2H4(g) ①
2CH4(g)?C2H4(g)+2H2(g) ②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)=CH4(g);△H=-Q1 kJ/mol
C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g);△H=-Q2 kJ/mol
C(s)+H2(g)=$\frac{1}{2}$C2H4(g);△H=-Q3 kJ/mol
Q1、Q2、Q3均为正值,下列关系正确的是( )
| A. | Q1>Q3>Q2 | B. | Q1>Q2>Q3 | C. | Q2>Q1>Q3 | D. | Q3>Q1>Q2 |
(2)量取反应物时,取50mL 0.50mol•L-1的盐酸,还需加入的试剂是B.
A.50mL 0.50mol•L-1 NaOH溶液 B.50mL 0.55mol•L-1 NaOH溶液
C.1.0g NaOH固体
(3)实验时大烧杯上若不盖硬纸板,求得的中和热数值偏小(填偏大、偏小、无影响)
(4)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如表所示.
| 反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热/kJ•mol-1 |
| A.1.0mol/L HCl溶液50mL、1.1mol/L NaOH溶液50mL | 13.0 | 19.8℃ | △H1 |
| B.1.0mol/L HCl溶液50mL、1.1mol/L NH3•H2O溶液50mL | 13.0 | 19.3℃ | △H2 |
②△H1≠△H2原因是NaOH是强碱,NH3•H2O是弱碱电离吸热.

| A. | 可用NaOH和湿润的红色的石蕊试纸检验NH4+ | |
| B. | 该方法会导致水体pH下降 | |
| C. | 该方法中O2做氧化剂,微生物做还原剂 | |
| D. | 处理后的废水需进一步处理才能排放 |

| A. | 有弱酸性,与Na2CO3、NaHCO3溶液均能反应 | |
| B. | 在一定条件下,1 mol该物质最多能与3 mol NaOH完全反应 | |
| C. | 在一定条件下,该物质可以发生取代、加成、水解、消去反应 | |
| D. | 该有机物分子中所有碳原子可能共平面 |
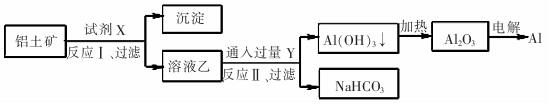
| A. | 试剂X为稀硫酸 | |
| B. | 反应Ⅱ中生成Al(OH)3的反应为:CO2+AlO2-+2H20=Al(OH)3↓+HCO3一 | |
| C. | 结合质子( H+)的能力由强到弱的顺序是Al02->CO32->OH- | |
| D. | Al2O3熔点很高,工业上还可采用电解熔融AICl3冶炼Al |
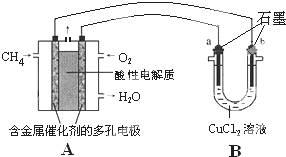 (3)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图.
(3)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图.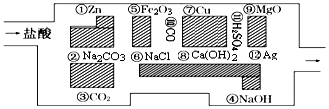
 .其中氧化剂是HCl,还原剂是Zn.
.其中氧化剂是HCl,还原剂是Zn.