题目内容
7.按要求填空(1)N原子的结构示意图为
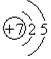
(2)含有相同氧原子数的NO和NO2,物质的量比为2:1,质量比为30:23,电子数目比为30:23
(3)在①漂白粉 ②MgCl2③食盐水 ④氯气 ⑤铁 ⑥Na2O ⑦稀硫酸 ⑧CO2 ⑨液氨 ⑩酒精 中属于电解质的是B(填选项,下同),属于非电解质的是D.
A.①②B.②⑥C.②③⑥D.⑧⑨⑩E.⑧⑨F.④⑧⑩
分析 (1)N原子的核电荷数=核外电子总数=7,最外层含有7个电子;
(2)NO和NO2分子分别含有1个O原子、2个O原子,含有相同氧原子数的NO和NO2,物质的量比为2:1,根据m=nM计算二者质量之比;根据二者含有电子数计算出电子数目之比;
(3)在水溶液中或熔化状态上能导电的化合物称为电解质,在上述两种情况下都不能导电的化合物称为非电解质,据此进行解答.
解答 解:(1)N原子的核电荷数、核外电子总数都是7,其原子结构示意图为: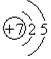 ,故答案为:
,故答案为: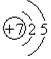 ;
;
(2)NO和NO2分子分别含有1个O原子、2个O原子,含有相同氧原子数的NO和NO2,二者物质的量比为2:1,二者质量之比=2mol×30g/mol:1mol×46g/mol=30:23;二者含有电子数之比=含有电子的物质的量之比=(15×2):(23×1)=30::23,
故答案为:2:1; 30:23;30:23;
(3)根据电解质的定义,在水溶液中或熔化状态上能导电的化合物称为电解质,在上述两种情况下都不能导电的化合物称为非电解质,所以在上述物质中属于电解质的是②⑥,即B正确;属于非电解质的是⑧⑨⑩,即D正确,
故答案为:B;D.
点评 本题考查了物质的量的计算、电解质与非电解质的判断及原子结构示意图等知识,题目难度中等,注意掌握物质的量与其它物理量之间的关系,明确电解质与非电解质的判断方法,试题培养了学生的灵活应用能力.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
17.已知下列三种气态物质之间的反应:
C2H2(g)+H2(g)?C2H4(g) ①
2CH4(g)?C2H4(g)+2H2(g) ②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)=CH4(g);△H=-Q1 kJ/mol
C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g);△H=-Q2 kJ/mol
C(s)+H2(g)=$\frac{1}{2}$C2H4(g);△H=-Q3 kJ/mol
Q1、Q2、Q3均为正值,下列关系正确的是( )
C2H2(g)+H2(g)?C2H4(g) ①
2CH4(g)?C2H4(g)+2H2(g) ②
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)=CH4(g);△H=-Q1 kJ/mol
C(s)+$\frac{1}{2}$H2(g)=$\frac{1}{2}$C2H2(g);△H=-Q2 kJ/mol
C(s)+H2(g)=$\frac{1}{2}$C2H4(g);△H=-Q3 kJ/mol
Q1、Q2、Q3均为正值,下列关系正确的是( )
| A. | Q1>Q3>Q2 | B. | Q1>Q2>Q3 | C. | Q2>Q1>Q3 | D. | Q3>Q1>Q2 |
18.工业上用铝土矿(主要成分为Al203,含Fe2O3等杂质)为原料冶炼铝的工艺流程如图:对上述流程中的判断正确的是( )
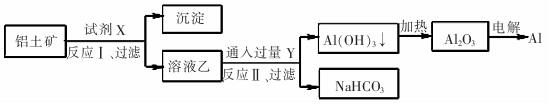

| A. | 试剂X为稀硫酸 | |
| B. | 反应Ⅱ中生成Al(OH)3的反应为:CO2+AlO2-+2H20=Al(OH)3↓+HCO3一 | |
| C. | 结合质子( H+)的能力由强到弱的顺序是Al02->CO32->OH- | |
| D. | Al2O3熔点很高,工业上还可采用电解熔融AICl3冶炼Al |
16.为了防治环境污染并对尾气进行综合利用,某硫酸厂用氨水吸收尾气中的SO2,再向吸收液中加入浓硫酸,以回收高浓度的SO2并得到副产品化肥(NH4)2SO4和NH4HSO4.为测定上述(NH4)2SO4和NH4HSO4固体混合物的组成,现称取该样品四份,分别加入相同浓度的NaOH溶液各40.00mL,加热至120℃左右,使氨气全部逸出[已知:(NH4)2SO4和NH4HSO4的分解温度均高于200℃],测得有关实验数据如下(标准状况):
(1)测定过程中有关反应的离子方程式为H++OH-=H2O、NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(2)3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为0.84L.
(3)试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比.
(4)欲计算该NaOH溶液的物质的量浓度应选择第Ⅲ组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程.
| 实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L |
| Ⅰ | 7.4 | 40.00 | 1.68 |
| Ⅱ | 14.8 | 40.00 | 3.36 |
| Ⅲ | 22.2 | 40.00 | 1.12 |
| Ⅳ | 37.0 | 40.00 | 0 |
(2)3.7g该样品进行同样实验时,生成的氨气在标准状况下体积为0.84L.
(3)试求算该混合物中(NH4)2SO4和NH4HSO4的物质的量之比.
(4)欲计算该NaOH溶液的物质的量浓度应选择第Ⅲ组数据,并由此计算NaOH溶液的物质的量浓度,写出计算过程.
 ;Al与NaOH溶液反应的离子方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
;Al与NaOH溶液反应的离子方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑. 酸碱中和在化工生产中有着重要应用.
酸碱中和在化工生产中有着重要应用.
 .其中氧化剂是HCl,还原剂是Zn.
.其中氧化剂是HCl,还原剂是Zn.