题目内容
7.反应X(g)+Y(g)?2Z(g)△H<0,达到平衡时,下列说法正确的是( )| A. | 减小容器体积,平衡向右移动 | |
| B. | 加入催化剂,平衡不移动故正逆反应速率不变 | |
| C. | 增大c(X),X的转化率增大 | |
| D. | 降低温度,Y的转化率增大 |
分析 A.减小容器体积,压强增大,该反应为气体体积不变的反应;
B.催化剂同等程度改变反应速率;
C.增大c(X),促进Y的转化;
D.△H<0,为放热反应,降低温度,平衡正向移动.
解答 解:A.减小容器体积,压强增大,该反应为气体体积不变的反应,则平衡不移动,故A错误;
B.催化剂同等程度改变反应速率,但平衡不移动,故B错误;
C.增大c(X),促进Y的转化,Y的转化率增大,但X的转化率减小,故C错误;
D.△H<0,为放热反应,降低温度,平衡正向移动,则Y的转化率增大,故D正确;
故选D.
点评 本题考查化学平衡移动,为高频考点,把握化学平衡移动的影响因素为解答的关键,侧重分析与应用能力的考查,注意温度、浓度、压强、催化剂对平衡的影响,选项C为易错点,题目难度不大.

练习册系列答案
相关题目
17.体积完全相同的两个容器A和B,已知A装有SO2和O2各1g,B装有SO2和O2各2g,在相同温度下反应达到平衡时A中SO2的浓度a,B中SO2的浓度b,则A,B两容器中SO2浓度的关系正确的是( )
| A. | a=b | B. | a<b<2a | C. | 2a=b | D. | 2a<b |
18.298K时,在容积不变的密闭容器中注满NO2气体,2NO2(g)?N2O4(g)△H<0.平衡后把该容器置于冰水中,下列性质或数值不会改变的是( )
①平均摩尔质量 ②质量 ③颜色 ④压强 ⑤各组分的质量分数⑥密度.
①平均摩尔质量 ②质量 ③颜色 ④压强 ⑤各组分的质量分数⑥密度.
| A. | ②⑥ | B. | ②③ | C. | ④⑤ | D. | ①⑥ |
15.已知反应:
①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1;
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列结论正确的是( )
①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1;
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列结论正确的是( )
| A. | .碳的燃烧热△H=-110.5 kJ•mol-1 | |
| B. | .①的反应热为221 kJ•mol-1 | |
| C. | 浓硫酸与稀NaOH溶液反应生成1 mol水,放出的热量为57.3 kJ | |
| D. | .碳的燃烧热大于110.5 kJ•mol-1 |
19.下列有关阿伏加德罗常数(NA)的说法错误的是( )
| A. | 32克O2所含的原子数目为2NA | |
| B. | 0.5molH2O含有的原子数目为1.5NA | |
| C. | 1molH2O含有的H2O分子数目为NA | |
| D. | 0.5NA个氯气分子的物质的量是1mol |
16.已知2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,关于该反应的下列说法错误的是( )
| A. | 该反应是一个放热反应 | |
| B. | 参加反应的氢气和氧气的总能量高于反应生成的水的总能量 | |
| C. | 在该化学反应中,破坏旧化学键吸收的能量大于形成新化学键释放的能量 | |
| D. | 发生反应时,断开反应物中的H-H键和O-O键都要吸收能量 |
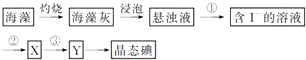

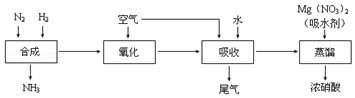
 某学校课外学习活动小组针对教材中铜与浓硫酸反应,提出了探究“能够与铜反应的硫酸的最低浓度是多少?”的问题,并设计了如下方案进行实验:
某学校课外学习活动小组针对教材中铜与浓硫酸反应,提出了探究“能够与铜反应的硫酸的最低浓度是多少?”的问题,并设计了如下方案进行实验: