题目内容
7.某同学按如图所示的装置进行电解实验.下列说法正确的是( )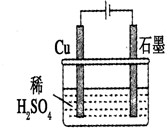
| A. | 石墨是电解池的负极,Cu是电解池的正极 | |
| B. | 电解过程中,铜电极上自身没什么变化 | |
| C. | 电解一定时间后,石墨电极上会有铜析出 | |
| D. | 整个电解过程中,溶液的pH不会变化 |
分析 根据图知,电解时,阳极上电极反应式为Cu-2e-=Cu2+、阴极上电极反应为2H++2e-=H2↑,当溶液中铜离子达到一定程度后,阴极上铜离子放电生成铜,以此解答该题.
解答 解:A、电解初期,石墨作阴极,Cu是电解池的阳极,故A错误;
B、电解时,阳极上电极反应式为Cu-2e-=Cu2+,所以铜电极不断溶解,故B错误;
C.电解初期,石墨作阴极,阴极上电极反应为2H++2e-=H2↑,当溶液中铜离子达到一定程度后,阴极上铜离子放电生成铜,所以石墨电极上先放出氢气后析出铜,故C正确;
D.阳极上电极反应式为Cu-2e-=Cu2+、阴极上电极反应为2H++2e-=H2↑,溶液中氢离子浓度减小,则PH增大,故D错误.
故选C.
点评 本题考查了电解原理,为高频考点,侧重于学生的分析能力的考查,注意把握阴阳极上发生的反应,活泼金属作阳极时,阳极上金属失电子而不是溶液中阴离子失电子,为易错点,难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
17.下列有关金属及其合金的说法不正确的是( )
| A. | 目前我国流通的硬币是由合金材料制造的 | |
| B. | 锡青铜的熔点比纯铜高 | |
| C. | 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 | |
| D. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
18.下列有关叙述正确的是( )
| A. | Cl2、SO2均能使品红溶液褪色,说明二者均有漂白性 | |
| B. | 元素周期表中第IA族全部是金属元素 | |
| C. | 盛有浓硫酸的烧杯敞口放置一段时间后,质量增加 | |
| D. | 硫在纯氧中的燃烧产物是三氧化硫 |
15.下列物质的电子式错误的是( )
| A. | 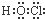 | B. | 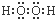 | C. | 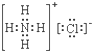 | D. | 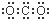 |
12.四种短周期主族元素在周期表中的相对位置如图所示,下列说法不正确的是( )
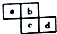

| A. | 原子半径:c>d>a>b | |
| B. | 原子序数d可能是a的3倍 | |
| C. | 最高价含氧酸的酸性c可能比d强 | |
| D. | 四种元素的氢化物可能是18电子分子 |
19.设NA为阿伏伽德罗常数,下列说法一定正确的是( )
| A. | 4g D2和足量O2反应可生成D2O 2NA个 | |
| B. | 98g H3PO4和H2SO4的混合物中含氢原子2.5NA个 | |
| C. | 6.02×1023个葡萄糖分子约含羟基6NA个 | |
| D. | 1molNa完全燃烧可转移电子NA个 |
9.福岛核电站泄漏的放射性物质中含有$\stackrel{131}{53}$I,下列有关$\stackrel{131}{53}$I的说法正确的是( )
| A. | 由此可确定碘元素的相对原子质量为131 | |
| B. | $\stackrel{131}{53}$I是碘元素的一种同位素 | |
| C. | $\stackrel{131}{53}$I核素中含中子数为53 | |
| D. | $\stackrel{131}{53}$I2的摩尔质量为262 g |