题目内容
18.下列有关叙述正确的是( )| A. | Cl2、SO2均能使品红溶液褪色,说明二者均有漂白性 | |
| B. | 元素周期表中第IA族全部是金属元素 | |
| C. | 盛有浓硫酸的烧杯敞口放置一段时间后,质量增加 | |
| D. | 硫在纯氧中的燃烧产物是三氧化硫 |
分析 A、氯气和二氧化硫具有漂白性,氯气利用的是次氯酸的强氧化性,二氧化硫利用的是结合有色物质形成不稳定的无色物质;
B、元素周期表中第IA族中的氢是非金属;
C、浓硫酸具有吸水性;
D、硫在氧气中氧化生成二氧化硫.
解答 解:A、Cl2、SO2均能使品红溶液褪色,氯气和水反应生成次氯酸具有漂白性,把有色物质氧化为无色物质,二氧化硫是结合有色物质形成不稳定的无色物质,加热恢复原来的颜色,未发生氧化还原反应,故D错误;
B、元素周期表中第IA族中的氢是非金属,不全是金属,故B错误;
C、浓硫酸具有吸水性,所以盛有浓硫酸的烧杯敞口放置一段时间后,质量增加,故C正确;
D、硫在氧气中氧化生成二氧化硫,而不是三氧化硫,故D错误;
故选C.
点评 本题综合考查元素化合物知识,涉及元素周期律、漂白作用原理和浓硫酸的性质等知识的考查,为高考高频考点,侧重于基础知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 0.1 mol金属钠变为钠离子时失去的电子数为NA | |
| B. | 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA | |
| C. | 0.1mol/L的MgCl2溶液中,含有Mg2+数目为0.1NA | |
| D. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3 NA |
3.下列物质的类别与所含能团都正确的是( )
(1) 酚类-OH
酚类-OH
(2) 羧酸-COOH--
羧酸-COOH--
(3) 醛类
醛类
(4)CH3-O-CH3醚类
(5 酯类
酯类
(1)
 酚类-OH
酚类-OH(2)
 羧酸-COOH--
羧酸-COOH--(3)
 醛类
醛类
(4)CH3-O-CH3醚类

(5
 酯类
酯类
| A. | (1)(2)(3)(4)(5) | B. | (2)(4) | C. | (2)(3)(4) | D. | (2)(4)(5) |
7.某同学按如图所示的装置进行电解实验.下列说法正确的是( )
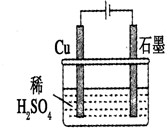

| A. | 石墨是电解池的负极,Cu是电解池的正极 | |
| B. | 电解过程中,铜电极上自身没什么变化 | |
| C. | 电解一定时间后,石墨电极上会有铜析出 | |
| D. | 整个电解过程中,溶液的pH不会变化 |
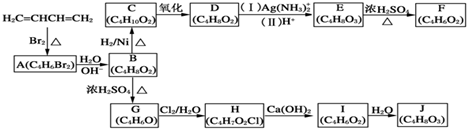
 +H2O,
+H2O,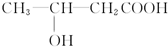 和
和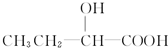 以外,还有
以外,还有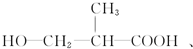 、
、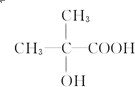 (写出结构简式,不考虑立体异构).
(写出结构简式,不考虑立体异构). ;
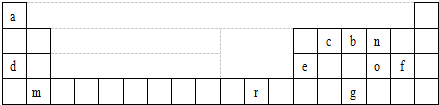
;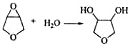 .
.
 ;
;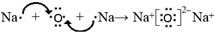 ;
;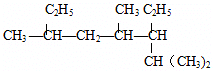 名称:2,4,6-三甲基-3-乙基辛烷
名称:2,4,6-三甲基-3-乙基辛烷 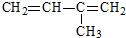 名称:2-甲基-1,3-丁二烯
名称:2-甲基-1,3-丁二烯
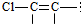 结构的有4种
结构的有4种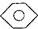 和
和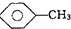 :KMnO4(H+)溶液.
:KMnO4(H+)溶液.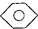 ,
,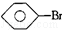 和C6H12(已烯):溴水.
和C6H12(已烯):溴水. ,CCl4和乙醇:水.
,CCl4和乙醇:水.