题目内容
12. 目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究.已知在不同温度下的化学反应平衡常数(K1、K2、K3)如表所示:
目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究.已知在不同温度下的化学反应平衡常数(K1、K2、K3)如表所示:目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究.已知在不同温度下的化学反应平衡常数(K1、K2、K3)如表所示:
| 化学反应 | 焓变 | 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |||
| ①2H2(g)+CO(g)?CH3OH(g) | △H1 | K1 | 2.5 | 0.34 | 0.15 |
| ②CO2(g)+H2(g)?CO(g)+H2O(g) | △H2 | K2 | 1.0 | 1.70 | 2.52 |
| ③CO2(g)+3H2(g)?CH3OH(g)+H2O(g) | △H3 | K3 | |||
(1)反应②是吸热(填“吸热”或“放热”)反应.
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1×K2 (用K1、K2表示),
△H3═△H1+△H2 (用△H1、△H2表示);根据反应③判断△S<0(填“>”、“=”或“<”),在较低(填“较高”或“较低”)温度下有利于该反应自发进行.
(3)要使反应③在一定条件下建立的平衡正向移动,可采取的措施有ADF(填写字母序号).
A.缩小反应容器的容积 B.扩大反应容器的容积 C.升高温度
D.降低温度 E.使用合适的催化剂 F.从平衡体系中及时分离出CH3OH
(4)500°C时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol•L-1、0.3mol•L-1、0.3mol•L-1、0.15mol•L-1,则此时v正<v逆(填“>”、“=”或“<”).
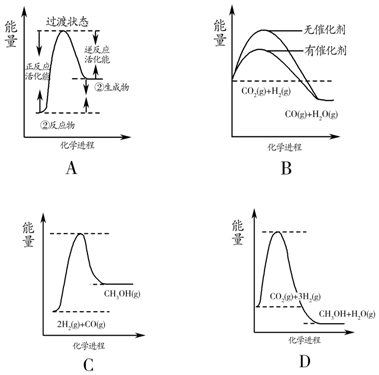
(5)根据表格测得焓变,下列能量关系图合理的是AD.
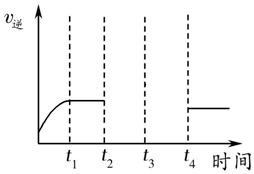
(6)某兴趣小组研究反应②的逆反应速率在下列不同条件下随时间的变化曲线,开始时升温,t1时平衡,t2时降压,t3时增加CO浓度,t4时又达到平衡.请画出t2至t4的曲线.
分析 (1)反应②平衡常数随温度升高增大,说明升高温度平衡正向进行,正反应是吸热反应;
(2)反应③是气体体积减小的反应△S<0,分析反应特征可知平衡常数K3=K1×K2,计算不同温度下反应③的平衡常数,结合温度变化分析判断反应焓变△H<0,依据反应①+②得到反应③,所以平衡常数K3=K1×K2;所以△H3═△H1+△H2;
(3)A.缩小反应容器的容积,压强增大,平衡向气体体积减小的方向移动;
B.扩大反应容器的容积,压强减小,平衡向气体增大的方向移动;
C.升高温度,平衡向吸热反应方向移动,根据K3=K1×K2判断温度对平衡移动影响;
D.由于K3=K1×K2,由表中数据可知,降低温度平衡常数增大,平衡正向移动;
E.使用合适的催化剂,不影响平衡移动;
F.从平衡体系中及时分离出CH3OH,平衡正向移动;
(4)500℃时K3=K1×K2=2.5,再计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行,进而判断v(正)、v(逆)相对大小;
(5)依据反应能量变化结合平衡移动原理和影响因素分析选项;
(6)依据影响化学反应速率的因素分析判断反应速率变化和反应进行方向绘制图象.
解答 解:(1)反应②平衡常数随温度升高增大,说明升高温度平衡正向进行,正反应是吸热反应,
故答案为:吸热;
(2)反应①+②可得反应③,则平衡常数K3=K1×K2,反应③是气体体积减小的反应△S<0,反应③3H2(g)+CO2(g)═CH3OH(g)+H2O(g)是气体体积减小的反应△S<0,分析反应特征可知平衡常数K3=K1×K2,计算不同温度下反应③的平衡常数,500°C时,K3=K1×K2=2.5×1.0=2.5,800°C时,K3=K1×K2=2.52×0.15=0.375,结合温度变化分析,随温度升高,平衡常数减小,平衡逆向进行,所以判断反应是放热反应,焓变△H<0,所以反应在低温下能自发进行,依据反应①+②得到反应③,所以平衡常数K3=K1×K2;所以△H3═△H1+△H2;
故答案为:K1×K2;△H3═△H1+△H2;<;较低;
(3)A.缩小反应容器的容积,缩小反应容器的容积,压强增大,平衡向正向移动,故正确;
B.扩大反应容器的容积,扩大反应容器的容积,压强减小,平衡逆向移动,故错误;
C.由于K3=K1×K2,由表中数据可知,升高温度平衡常数减小,平衡逆向移动,故错误;
D.由于K3=K1×K2,由表中数据可知,降低温度平衡常数增大,平衡正向移动,故正确;
E.使用合适的催化剂,可以加快反应速率,但不影响平衡移动,故错误;
F.从平衡体系中及时分离出CH3OH,生成物浓度减小,平衡正向移动,故正确,
故选:ADF;
(4)500℃时K3=K1×K2=2.5,浓度商Qc=$\frac{0.3×0.15}{0.1×0.{3}^{3}}$=16>K=2.5,反应向逆反应进行,故v(正)<v(逆),
故答案为:<;
(5)A、反应②已经平衡常数随温度变化分析为吸热反应,反应物能量低于生成物,图象符合,故A正确;
B、催化剂改变反应速率不改变化学平衡,平衡状态不变,图象不符合,故B错误;
C、①2H2(g)+CO(g)?CH3OH(g),依据数据分析,平衡常数随温度 升高减小,说明正反应为放热反应,反应物能量高于生成物,图象不符合,故C错误;
D、反应③3H2(g)+CO2(g)═CH3OH(g)+H2O(g)是放热盐,反应物能量高于生成物,图象符合,故D正确;
故答案为:AD;
(6)反应②CO2(g)+H2(g)?CO(g)+H2O(g)是气体体积不变的吸热反应,反应的逆反应速率在下列不同条件随时间的变化曲线,开始时升温,逆反应速率增大,t1时平衡,t2时降压,逆反应速率减小,平衡不变,t3时增加CO浓度,此时刻逆反应速率增大,随反应进行减小,大平衡状态大于t2-t3平衡状态的逆反应速率,t4时又达到平衡,依据反应速率影响分析绘制出去下变化;画出t2至t4的曲线为如图所示 ;
;
故答案为: .
.
点评 本题考查了化学平衡、反应速率影响因素分析判断,平衡常数计算应用,掌握反应特征和平衡移动原理是关键,题目难度中等.

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案| A. | 推广使用燃煤脱硫技术,防治SO2污染 | |
| B. | 使用天然气热水器取代电热水器 | |
| C. | 推荐使用手帕,尽量减少使用面纸 | |
| D. | 在建筑、布展、运营过程中应用大规模的太阳能光伏发电系统 |
| A. | 向0.1 mol•L-1CH3COOH溶液中加入少量水,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 | |
| B. | 在0.l mol•L-1的稀硫酸加水稀释的过程中,c(H+):c(SO42-)始终为2:1 | |
| C. | 向盐酸中加入氨水至中性,溶液中$\frac{c(N{H}_{4}^{+})}{c(c{l}^{-})}$>1 | |
| D. | 在含0.1mol NaHSO4溶液中:c(H+)=c(SO42-)+c(OH-) |
| A. | 乙烯、苯、环己烷都属于脂肪烃 | B. | 苯、环戊烷、环己烷同属于芳香烃 | ||
| C. | 乙烯、乙炔同属于烯烃 | D. |  、 、 、 、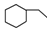 同属于环烷烃 同属于环烷烃 |
| A. | 在常温常压下,0.5 mol任何气体的体积都必定是11.2 L | |
| B. | 在标准状况下,1 mol任何物质的体积都约是22.4 L | |
| C. | 常温常压下,1 mol任何气体的体积都约是22.4 L | |
| D. | 在标准状况下,0.5 mol CO2所占有的体积约是11.2 L |
| A. | Mg(OH)2 | B. | Al(OH)3 | C. | NaHCO3 | D. | MgCO3 |