题目内容
2.用NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 标准状况下,4.48 L重水(D2O)中含有的中子数为2NA | |
| B. | 0.1mol乙烯和乙醇(C2H5OH,蒸汽)混合物完全燃烧所消耗的氧分子数一定为0.3NA | |
| C. | 常温常压下,15g乙烷分子中含有的共价键数目为3NA | |
| D. | 273K,101kPa下,14g乙烯与丙烯混合物中含有碳原子数目为3NA |
分析 A、标况下重水为液体;
B、1mol乙烯和1mol乙醇燃烧均消耗3mol氧气;
C、求出乙烷的物质的量,然后根据根据乙烷中含7条共价键来分析;
D、乙烯和丙烯的最简式均为CH2,求出混合物中含有的CH2的物质的量,然后根据CH2中含1个碳原子来分析.
解答 解:A、标况下重水为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、1mol乙烯和1mol乙醇燃烧均消耗3mol氧气,故0.1mol乙烯和乙醇蒸汽的混合气体燃烧消耗0.3mol氧气即0.3NA个氧气分子,故B正确;
C、15g乙烷的物质的量为n=$\frac{m}{M}=\frac{15g}{30g/mol}$=0.5mol,而乙烷中含7条共价键,故0.5mol乙烷中含3.5NA条共价键,故C错误;
D、乙烯和丙烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量n=$\frac{14g}{14g/mol}$=1mol,而CH2中含1个碳原子,故1molCH2中含NA个碳原子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
13.一定条件下,乙烷发生分解反应:C2H6?C2H4+H2.一段时间后,反应达到平衡状态,这说明( )
| A. | 反应完全停止 | B. | 各物质的浓度保持不变 | ||
| C. | 反应物消耗完全 | D. | 正反应速率大于逆反应速率 |
10.在含有大量H+、Ca2+、Cl-的溶液中,还能大量共存的离子是 ( )
| A. | OH- | B. | NO3- | C. | CO32- | D. | Ag + |
17.下列化学用语表述正确的是( )
| A. | 氯气的电子式: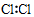 | B. | 氮气的结构式: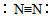 | ||
| C. | F一的结构示意图: | D. | H2O2的电子式: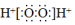 |
7.表是元素周期表的一部分,其中A、B、D、E、G、J为短周期元素,G元素的核电荷数为B元素的2倍.请回答下列问题:
(1)J的最高价氧化物对应水化物的化学式是HClO4.
(2)G2J2常用作橡胶的低温硫化剂和黏结剂,其电子式为 .写出一个能表示元素G、J非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓或Na2S+Cl2=2NaCl+S↓.
.写出一个能表示元素G、J非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓或Na2S+Cl2=2NaCl+S↓.
(3)G单质在空气中燃烧生成一种无色有刺激性气味的气体,该无色有刺激性气味的气体与含1molJ的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在-定条件下反应,可生成一种强酸和一种氧化物,且该反应中有NA个电子转移,则该反应的化学方程式是SO2+2HClO3$\frac{\underline{\;一定条件\;}}{\;}$H2SO4+2ClO2.
(4)A的最简单氢化物是极性(填“极性”或“非极性”)分子,实验室制备该物质的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O或NH3•H2O$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(5)根据元素周期律,可以推测上表中长周期元素的单质具有半导体特性的是Ge、As(填元素符号).
| A | B | ||
| D | E | G | J |
| L | M | Q |
(2)G2J2常用作橡胶的低温硫化剂和黏结剂,其电子式为
 .写出一个能表示元素G、J非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓或Na2S+Cl2=2NaCl+S↓.
.写出一个能表示元素G、J非金属性强弱关系的化学方程式H2S+Cl2=2HCl+S↓或Na2S+Cl2=2NaCl+S↓.(3)G单质在空气中燃烧生成一种无色有刺激性气味的气体,该无色有刺激性气味的气体与含1molJ的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在-定条件下反应,可生成一种强酸和一种氧化物,且该反应中有NA个电子转移,则该反应的化学方程式是SO2+2HClO3$\frac{\underline{\;一定条件\;}}{\;}$H2SO4+2ClO2.
(4)A的最简单氢化物是极性(填“极性”或“非极性”)分子,实验室制备该物质的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O或NH3•H2O$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(5)根据元素周期律,可以推测上表中长周期元素的单质具有半导体特性的是Ge、As(填元素符号).
14.现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p2; ②1s22s22p63s23p3; ③1s22s22p3; ④1s22s22p4.则下列有关比较中正确的是( )
| A. | 电负性:④>③>②>① | B. | 原子半径:④>③>②>① | ||
| C. | 第一电离能:④>③>②>① | D. | 最高正化合价:④>③>②>① |
11.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 1标准大气压下原子数为NA的水蒸气为1mol | |
| B. | 1L1mol/L的NaOH溶液中Na+的物质的量为1mol | |
| C. | 标准状况下,22.4L氦气的质量为4g | |
| D. | 用含1molHCl的盐酸制取氯气,氯元素失去的电子数为4NA |