题目内容
KMnO4可与盐酸反应生成Cl2,方程式如下:请把物质补充完整并配平.
KMnO4+ HCl= MnCl2+ Cl2↑+ KCl+ H2O.
考点:氧化还原反应方程式的配平
专题:氧化还原反应专题
分析:该反应中Mn元素化合价由+7价变为+2价、部分Cl元素化合价由-1价变为0价、部分Cl元素化合价不变,其转移电子总数为10,根据元素守恒知□中物质为KCl,再结合原子守恒配平方程式,据此分析解答.
解答:
解:该反应中Mn元素化合价由+7价变为+2价、部分Cl元素化合价由-1价变为0价、部分Cl元素化合价不变,根据元素守恒知□中物质为KCl,其转移电子总数为10,则MnCl2的计量数是2、Cl2的计量数是5,再结合原子守恒配平方程式为2KMnO4+16HCl=2MnCl2+5Cl2↑+2KCl+8H2O,
故答案为:2;16;2;5;2;8.
故答案为:2;16;2;5;2;8.
点评:本题考查氧化还原反应配平,该反应中HCl体现还原性和酸性,根据生成物中元素化合价变化配平方程式较简便,知道常见元素化合价,题目难度不大.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
某元素电子构型为[Xe]4f46s2,其应在( )
| A、s区 | B、p区 | C、d区 | D、f区 |
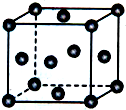 已知X、Y、Z为短周期元素,X、Y同周期,X和Z同主族,Y原子基态时2p轨道上的未成对电子数最多,X的低价氧化物和Y单质分子的电子数相等.W2+的核外电子排布简式为[Ar]3d9.
已知X、Y、Z为短周期元素,X、Y同周期,X和Z同主族,Y原子基态时2p轨道上的未成对电子数最多,X的低价氧化物和Y单质分子的电子数相等.W2+的核外电子排布简式为[Ar]3d9.