题目内容
某元素电子构型为[Xe]4f46s2,其应在( )
| A、s区 | B、p区 | C、d区 | D、f区 |
考点:原子核外电子排布,元素周期表的结构及其应用
专题:原子组成与结构专题,元素周期律与元素周期表专题
分析:s区的外围电子排布为nsx(氦除外),包含第ⅠA、ⅡA族元素,
p区的外围电子排布为ns2npx(包含氦氦元素,氦除外),包含ⅢA~ⅦA族元素与零族元素,
ds区的外围电子排布为nd10(n+1)sx,包含ⅠB、ⅡB元素,
d区的外围电子排布为ndx (n+1)sy,x不等于10,包含ⅢB~ⅦB族元素与第Ⅷ族元素,
f区外围电子排布为(n-2)f1~14 ns1~2,包括镧系和锕系,据此判断.
p区的外围电子排布为ns2npx(包含氦氦元素,氦除外),包含ⅢA~ⅦA族元素与零族元素,
ds区的外围电子排布为nd10(n+1)sx,包含ⅠB、ⅡB元素,
d区的外围电子排布为ndx (n+1)sy,x不等于10,包含ⅢB~ⅦB族元素与第Ⅷ族元素,
f区外围电子排布为(n-2)f1~14 ns1~2,包括镧系和锕系,据此判断.
解答:
解:某元素电子构型为[Xe]4f46s2,该元素为Nd元素,符合处于f区外围电子排布为(n-2)f1~14 ns1~2,处于周期表第六周期ⅢB族的镧系,处于f区,
故选D.
故选D.
点评:本题考查结构与物质关系,难度不大,注意掌握元素周期表中各区的划分.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列实验中,金属或固体可以完全溶解的是( )
| A、在H2O2溶液中加入少量MnO2粉末 |
| B、镀锌铁皮加入足量的NaOH溶液中 |
| C、1mol铜片与含2mol H2SO4的浓硫酸共热 |
| D、常温下,1mol铜片投入含4mol HNO3的浓硝酸中 |
在核外电子排布如下的原子中,有最高化合价且其值最大的是( )
| A、1S22S22P2 |
| B、1S22S22P63S23P6 |
| C、1S22S22P5 |
| D、1S22S22P63S23P1 |
下列说法正确的是( )
| A、基态原子第四电子层只有2个电子,则该原子第三电子层的电子数肯定为8或18个 | ||
| B、Li、Be、B三种元素的第一电离能(I1)差别不大,而I2差别很大,则三种原子中最难失去第二个电子的是Be | ||
C、R为第二周期元素,其原子具有的电子层数为最外层电子数的
| ||
| D、核外电子数为奇数的基态原子,其原子轨道中一定含有未成对电子 |
下列原子或离子的基态电子排布式正确的是( )
| A、Ni:[Ar]3d8 |
| B、Cu:[Ar]3d94s2 |
| C、S2-:[Ne]2s23p6 |
| D、Si:[Ne]3s23p2 |

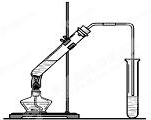 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题: