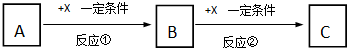
题目内容
19.某原电池的结构如图所示,下列有关该原电池的说法不正确的是( )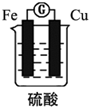
| A. | 该电池工作时电能转变为化学能 | B. | 铁片的质量变轻 | ||
| C. | 铜片上发生的反应2H++2e-=H2↑ | D. | SO42-向铁片移动 |
分析 由图可知,Fe作负极,Cu作正极,发生电池反应为Fe+2H+=Fe2++H2↑,原电池中阴离子向负极移动,原电池是将化学能转化为电能的装置,以此来解答.
解答 解:A.该电池工作时化学能转变为电能,故A错误;
B.Fe为负极,失去电子而溶解,则铁片的质量变轻,故B正确;
C.铜电极上氢离子得到电子生成氢气,发生的反应为2H++2e-=H2↑,故C正确;
D.Fe为负极,则SO42-向铁片移动,故D正确;
故选A.
点评 本题考查原电池,为高频考点,把握原电池的正负极、电极反应、电池反应为解答的关键,侧重分析与应用能力的考查,注意离子的移动方向,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
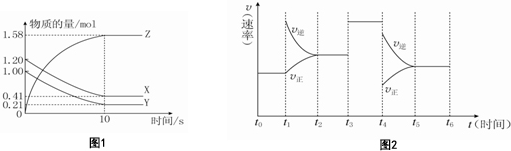
9.对于反应3X(g)+Y(g)?Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
(1)升高温度:增大;
(2)增大压强:增大;
(3)增大容器容积:减小.
(1)升高温度:增大;
(2)增大压强:增大;
(3)增大容器容积:减小.
4.卤族元素随着原子核电荷数的增加,下列叙述不正确的是( )
| A. | 原子半径依次增大 | B. | 单质的熔沸点逐渐升高 | ||
| C. | 卤离子的还原性逐渐减弱 | D. | 氢化物的热稳定性依次减弱 |
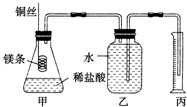 某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答下列问题.该小组设计的简单实验装置如图所示:
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答下列问题.该小组设计的简单实验装置如图所示: