题目内容
11.用15.8g高锰酸钾氧化密度为1.19g/cm3,质量分数为36.5%的盐酸以制取氯气.反应如下:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
求:(1)生成Cl2在标况下的体积;
(2)被KMnO4氧化的盐酸的体积;
(3)反应中转移的电子总数.
分析 (1)根据V=nVm来计算氯气的体积;
(2)根据反应的化学方程式计算,根据Cl元素化合价的变化可知,16molHCl参加反应时,有10molHCl被氧化;
(3)氧化还原反应中,化合价升高值=化合价降低值=转移电子数,根据化合价的变化结合物质的量来回答.
解答 解:(1)n(KMnO4)=$\frac{15.8g}{158g/mol}$=0.1mol,
2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 被氧化的HCl
2mol 16mol 5mol 10mol
0.1mol n(HCl) n(Cl2) n(HCl)被氧化
n(Cl2)=0.25mol,V(Cl2)nVm═0.25mol×22.4L/mol=5.6L,答:生成Cl2在标况下的体积是5.6L;
(2)则n(HCl)=0.8mol,n(HCl)被氧化=0.5mol,密度是1.19g/cm3、质量分数为36.5%的盐酸的物质的量浓度c=$\frac{1000×36.5%×1.19g/c{m}^{3}}{36.5g/mol}$=11.9mol/L,体积V=$\frac{n}{c}$=$\frac{0.5mol}{11.9mol/L}$≈0.042L=42mL,
答:15.8g KMnO4氧化的盐酸的体积是42mL;
(3)根据方程式,当消耗高锰酸钾2mol时,反应中转移的电子的物质的量是10mol,当0.1mol高锰酸钾参加反应,转移电子是0.5mol,即个数为3.01×1023,故答案为:3.01×1023或0.5NA.
答:反应中转移的电子总数是3.01×1023或0.5NA.
点评 本题考查化学方程式的计算,题目难度中等,注意有关反应的化学方程式以及物质的量的相关计算公式以及氧化还原反应中概念的运用.

| A. | 用FeCl3溶液腐蚀铜线路板:Fe3++3Cu═Fe2++3Cu2+ | |
| B. | 少量氨气中通入过量亚硫酸溶液中:NH3+H2SO3═NH4++HSO3- | |
| C. | Cl2与水反应生成盐酸和次氯酸:Cl2+H2O═H++Cl-+HClO | |
| D. | 小苏打溶液中加入过量的烧碱溶液:HCO3-+OH-═CO32-+H2O |
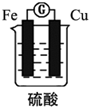
| A. | 该电池工作时电能转变为化学能 | B. | 铁片的质量变轻 | ||
| C. | 铜片上发生的反应2H++2e-=H2↑ | D. | SO42-向铁片移动 |
①热稳定性:H2O>HF>H2S ②结合质子能力:OH->CH3COO->Cl-
③酸性:H3PO4>H2SO4>HClO4 ④原子半径:Na>Mg>O( )
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
| A. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B. | 用澄清石灰水鉴别SO2 和CO2 | |
| C. | 将Fe(NO3)2 溶于稀盐酸,滴加KSCN 溶液没有颜色变化 | |
| D. | 透闪石的化学成分为Ca2Mg5Si8O22(OH)2 写成氧化物的形式为:2CaO•5MgO•8SiO2•H2O |
| A. | 已溶解的溶质和未溶解的溶质质量相等 | |
| B. | 溶质不再溶解,因此从表面看溶质不再减少,也不再增加 | |
| C. | 升高温度,饱和溶液将变为不饱和溶液 | |
| D. | 溶质的溶解和结晶继续进行,且速率相等 |
| A. | 在五水硫酸铜中滴加少量浓硫酸,固体颜色由蓝变白,说明浓硫酸具有吸水性 | |
| B. | 在未知试液中滴加BaCl2溶液得白色沉淀,取该白色沉淀加稀盐酸不溶解,说明原未知试液中含有SO42- | |
| C. | 在铜片上滴加少量稀硫酸,无明显现象,说明稀硫酸没有氧化性 | |
| D. | 某未知气体通入品红溶液中,品红溶液褪色,则原气体一定是 SO2 |
| A. | Na与水反应 Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向AlCl3溶液中加入过量的NaOH溶液 Al3++3OH-═Al(OH)3↓ | |
| C. | 氢氧化钡溶液与硫酸溶液反应 Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | CO2通入过量澄清石灰水 CO2+Ca2++2OH-═CaCO3↓+H2O |